Активни съставки: Норелгестромин / Етинилестрадиол
EVRA трансдермален пластир 203 микрограма норелгестромин / 24 часа + 33,9 микрограма етинилестрадиол / 24 часа
Защо се използва Evra? За какво е?
EVRA съдържа два вида полови хормони, прогестин, наречен норелгестромин и естроген, наречен етинил естрадиол.
Тъй като съдържа два хормона, EVRA се нарича "комбиниран хормонален контрацептив".
Използва се за предотвратяване на бременност.
Противопоказания Когато Evra не трябва да се използва
Преди да започнете да използвате EVRA, трябва да прочетете информацията за кръвни съсиреци в раздел 2. Особено важно е да прочетете симптомите на кръвен съсирек (вижте точка 2 "Кръвни съсиреци").
Не използвайте EVRA:
Не използвайте EVRA, ако имате някое от изброените по -долу състояния. Ако имате някое от изброените по -долу състояния, моля, свържете се с Вашия лекар. Вашият лекар ще обсъди с Вас други методи за контрол на раждаемостта, които може да са по -подходящи за Вас.
- ако имате (или някога сте имали) кръвен съсирек в кръвоносен съд на крака (дълбока венозна тромбоза, ДВТ), белия дроб (белодробна емболия, РЕ) или други органи;
- ако знаете, че имате нарушение, което засяга съсирването на кръвта, като например дефицит на протеин С, дефицит на протеин S, дефицит на антитромбин-III, фактор V Leiden или антифосфолипидни антитела;
- ако трябва да се подложите на операция или ако ще лежите дълго време;
- ако някога сте имали инфаркт или инсулт;
- ако имате (или някога сте имали) стенокардия (състояние, което причинява силна гръдна болка и може да бъде първи признак на инфаркт) или преходна исхемична атака (TIA - временни симптоми на инсулт);
- ако имате някое от следните заболявания, които биха могли да увеличат риска от образуване на кръвни съсиреци в артериите: - тежък диабет с увреждане на кръвоносните съдове - много високо кръвно налягане - много високо ниво на мазнини (холестерол или триглицериди) в кръвта - a заболяване, известно като хиперхомоцистеинемия
- ако имате (или някога сте имали) вид мигрена, наречена "мигрена с аура";
- ако сте алергични към норелгестромин, етинил естрадиол или към някоя от останалите съставки на това лекарство (изброени в точка 6)
- ако Ви е казано, че може да имате рак на гърдата или матката, шийката на матката или вагината
- ако някога сте имали чернодробни тумори или чернодробно заболяване, тъй като черният Ви дроб не работи правилно
- ако имате необяснимо вагинално кървене. Не използвайте това лекарство, ако попаднете в някоя от изброените по -горе ситуации. Ако не сте сигурни, попитайте Вашия лекар, фармацевт или медицинска сестра, преди да използвате това лекарство.
Кога трябва да се внимава с EVRA
Кога трябва да посетите лекар?
Спешно се свържете с лекар
Ако забележите възможни признаци на кръвен съсирек, които могат да показват, че страдате от кръвен съсирек в крака (дълбока венозна тромбоза), кръвен съсирек в белия дроб (белодробна емболия), инфаркт или инсулт (вижте раздел по -долу „Кръвен съсирек (тромбоза)“).
Предпазни мерки при употреба Какво трябва да знаете, преди да приемете Evra
Преди да използвате това лекарство, трябва да отидете на лекар за консултация.
Уведомете Вашия лекар, ако някое от следните се отнася за Вас.
Ако това състояние се появи или се влоши, докато използвате EVRA, трябва да уведомите Вашия лекар.
- ако имате болест на Crohn или улцерозен колит (хронично възпалително заболяване на червата); ако имате системен лупус еритематозус (SLE, заболяване, което засяга естествената защитна система);
- ако имате хемолитично -уремичен синдром (HUS, нарушение на кръвосъсирването, причиняващо бъбречна недостатъчност);
- ако имате сърповидно -клетъчна анемия (наследствено заболяване на червените кръвни клетки);
- ако имате високи нива на мазнини в кръвта (хипертриглицеридемия) панкреатит (възпаление на панкреаса);
- ако трябва да се подложите на операция или ако ще лежите дълго време;
- ако току -що сте родили, рискът от образуване на кръвни съсиреци е по -висок. Попитайте Вашия лекар колко време след раждането можете да започнете да приемате [изобретено име];
- ако имате „възпаление на вените под кожата (повърхностен тромбофлебит);
- ако имате разширени вени.
КРЪВНИ СЪСИРЕЦИ
Използването на комбиниран хормонален контрацептив като EVRA увеличава риска от образуване на кръвен съсирек в сравнение с неизползването му. В редки случаи кръвен съсирек може да блокира кръвоносните съдове и да причини сериозни проблеми.
Могат да се развият кръвни съсиреци
- във вените (наречени "венозна тромбоза", "венозна тромбоемболия" или ВТЕ)
- в артериите (наричани „артериална тромбоза“, „артериална тромбоемболия“ или АТЕ).
Възстановяването от кръвни съсиреци не винаги е пълно. Рядко могат да се появят дълготрайни тежки ефекти или много рядко те могат да бъдат фатални.
Важно е да запомните, че общият риск от вреден кръвен съсирек, свързан с EVRA, е нисък.
КАК ДА РАЗПОЗНАЕТЕ КРЪВЕН КРЪВ
Незабавно посетете лекар, ако забележите някой от следните признаци или симптоми.
- болка или болезненост в крака, които могат да се усетят само когато стоите или ходите
- повишено усещане за топлина в засегнатия крак
- промяна в цвета на кожата на крака, като например бледо, червено или синьо
- внезапен и необясним задух или учестено дишане;
- внезапна кашлица без очевидна причина, евентуално причиняваща отделяне на кръв;
- остра болка в гърдите, която може да се увеличи с дълбоко дишане;
- силно замайване или замаяност;
- ускорен или неравномерен сърдечен ритъм;
- силна болка в стомаха
- болка в гърдите, дискомфорт, чувство на натиск или тежест
- усещане за притискане или пълнота в гърдите, ръката или под гръдната кост;
- чувство на ситост, лошо храносмилане или задушаване;
- дискомфорт в горната част на тялото, излъчващ към гърба, челюстта, гърлото, ръцете и стомаха;
- изпотяване, гадене, повръщане или замаяност;
- крайна слабост, тревожност или задух;
- бърз или неравномерен сърдечен ритъм
- внезапно изтръпване или слабост на лицето, ръката или крака, особено от едната страна на тялото;
- внезапно объркване, трудности при говорене или разбиране;
- внезапно затруднено виждане в едното или в двете очи;
- внезапно затруднено ходене, замаяност, загуба на равновесие или координация;
- внезапна, тежка или продължителна мигрена без известна причина;
- загуба на съзнание или припадък със или без припадъци.
- подуване и бледосиньо обезцветяване на един "крайник";
- силна стомашна болка (остър корем)
КРЪВНИ КРЪВИ ВЪВ ВЕНА
Какво може да се случи, ако във вената се образува кръвен съсирек?
- Използването на комбинирани хормонални контрацептиви е свързано с повишен риск от образуване на кръвни съсиреци във вените (венозна тромбоза). Тези странични ефекти обаче са редки. В повечето случаи те се появяват през първата година от употребата на комбиниран хормонален контрацептив.
- Ако кръвен съсирек се образува във вена на крака или стъпалото, това може да причини дълбока венозна тромбоза (ДВТ).
- Ако кръвен съсирек пътува от крака и се засели в белия дроб, това може да причини "белодробна емболия".
- Много рядко съсирек може да се образува в друг орган като окото (тромбоза на вената на ретината).
Кога е най -висок рискът от образуване на кръвен съсирек във вена?
Рискът от образуване на кръвен съсирек във вена е най -висок през първата година от приемането на комбиниран хормонален контрацептив за първи път. Рискът може да бъде още по -висок, ако рестартирате приема на комбиниран хормонален контрацептив (същото лекарство или различно лекарство) след почивка от 4 или повече седмици.
След първата година рискът се намалява, но винаги е малко по -висок, отколкото ако не сте използвали комбиниран хормонален контрацептив.
Когато спрете приема на EVRA, рискът от образуване на кръвен съсирек се нормализира в рамките на няколко седмици.
Какъв е рискът от образуване на кръвен съсирек?
Рискът зависи от естествения ви риск от ВТЕ и от вида комбиниран хормонален контрацептив, който приемате.
Общият риск от развитие на кръвен съсирек в крака или белия дроб (DVT или PE) с EVRA е нисък.
- От 10 000 жени, които не използват никакви комбинирани хормонални контрацептиви и които не са бременни, около 2 ще развият кръвен съсирек за една година.
- От 10 000 жени, които използват комбиниран хормонален контрацептив, който съдържа левоноргестрел, норетистерон или норгестимат, около 5-7 ще развият кръвен съсирек за една година.
- От 10 000 жени, които използват комбиниран хормонален контрацептив, който съдържа етоноргестрел или норелгестромин, като EVRA, около 6-12 ще развият кръвен съсирек за една година.
- Рискът от образуване на кръвен съсирек зависи от вашата медицинска история
Риск от образуване на кръвен съсирек за една година
Жени, които не използват комбинирано хормонално хапче / пластир / пръстен и които не са бременни
Около 2 от 10 000 жени
Жени, използващи комбинирани хормонални контрацептиви, съдържащи левоноргестрел, норетистерон или норгестимат
Около 5-7 от 10 000 жени
Жени, които използват EVRA
Около 6-12 от 10 000 жени
Фактори, които увеличават риска от образуване на кръвен съсирек във вената
Рискът от образуване на кръвен съсирек с EVRA е нисък, но някои състояния го карат да се увеличи. Рискът му е по -голям:
- ако имате тежко наднормено тегло (индекс на телесна маса или ИТМ над 30 kg / m2);
- ако близък роднина е имал кръвен съсирек в крака, белия дроб или друг орган в млада възраст (по -малко от около 50 години). В този случай може да имате наследствено разстройство на кръвосъсирването;
- ако Ви предстои операция или ако трябва да лежите дълго време поради нараняване или заболяване или ако имате крак в гипс. Може да се наложи да спрете приема на EVRA няколко седмици преди операцията или по време на период, в който сте по -малко подвижни. Ако трябва да спрете приема на EVRA, попитайте Вашия лекар кога можете да започнете да го приемате отново;
- с напредване на възрастта (особено след 35 -годишна възраст);
- ако сте родили преди по -малко от няколко седмици.
Рискът от образуване на кръвен съсирек се увеличава, колкото повече състояния имате от този тип.
Пътуването със самолет (продължително> 4 часа) може временно да увеличи риска от образуване на кръвен съсирек, особено ако имате някои от изброените други рискови фактори.
Важно е да кажете на Вашия лекар, ако някое от изброените се отнася за Вас, дори ако не сте сигурни. Вашият лекар може да реши, че лечението с EVRA трябва да бъде спряно.
Уведомете Вашия лекар, ако някое от горните състояния се промени, докато използвате EVRA, например, ако близък роднина има тромбоза без известна причина или ако наддавате много.
КРЪВНИ КРЪВИ В АРТЕРИЯ
Какво може да се случи, ако кръвен съсирек се образува в "артерия"?
Подобно на кръвни съсиреци във вена, съсиреците в артерията могат да причинят сериозни проблеми, например могат да причинят инфаркт или инсулт.
Фактори, които увеличават риска от образуване на кръвен съсирек в артерията
Важно е да се отбележи, че рискът от инфаркт или инсулт, свързан с употребата на EVRA, е много нисък, но може да се увеличи:
- с увеличаване на възрастта (над 35 години);
- ако пушите. Когато използвате комбиниран хормонален контрацептив, като EVRA, се препоръчва да спрете да пушите. Ако не можете да спрете да пушите и сте на възраст над 35 години, Вашият лекар може да Ви посъветва да използвате различен вид контрацептив; ако сте с наднормено тегло;
- ако имате високо кръвно налягане;
- ако член на вашето близко семейство е имал инфаркт или инсулт в ранна възраст (по -малко от около 50 години). В този случай може да имате и висок риск от инфаркт или инсулт;
- ако вие или ваш близък роднина имате високо ниво на мазнини в кръвта (холестерол или триглицериди);
- ако страдате от мигрена, особено мигрена с аура;
- ако имате някакви сърдечни проблеми (дефект на клапана, нарушение на сърдечния ритъм, наречено предсърдно мъждене);
- ако имате диабет.
Ако имате повече от едно от тези състояния или ако някое от тях е особено тежко, рискът от образуване на кръвен съсирек може да бъде дори по -висок.
Уведомете Вашия лекар, ако някое от горните състояния се промени, докато използвате EVRA, например, ако започнете да пушите, ако близък роднина има тромбоза без известна причина или ако наддавате много.
В допълнение, говорете с Вашия лекар, фармацевт или медицинска сестра, преди да използвате EVRA, ако имате някое от следните състояния, или ако тези състояния се развият или влошат: ако мислите, че сте бременна
- ако имате главоболие, което се влошава или идва по -често
- ако тежите 90 кг или повече
- ако имате високо кръвно налягане или кръвно налягане, което има тенденция да се повишава
- ако имате заболяване на жлъчния мехур, включително камъни в жлъчката или възпаление на жлъчния мехур
- ако имате кръвно заболяване, наречено "порфирия"
- ако имате заболяване на нервната система, което причинява внезапни движения на тялото, наречени "хорея на Sydenham"
- ако сте имали "обрив с мехури (наречен" гестационен херпес ") по време на бременност
- ако имате загуба на слуха
- ако имате диабет
- ако имате депресия
- ако имате епилепсия или друго състояние, което може да причини гърчове
- ако имате чернодробни проблеми, които включват пожълтяване на кожата и бялото на очите (жълтеница)
- ако имате или сте имали „петна по бременност“. Това са жълто-кафяви петна, особено по лицето (наречени "хлоазма"). Тези петна може да не изчезнат напълно след спиране на EVRA. Защитете кожата си от слънчева светлина или ултравиолетово лъчение. Това може да предотврати появата на тези петна или да ги влоши
- ако имате бъбречни проблеми.
Ако не сте сигурни дали някое от горните състояния се отнася за Вас, говорете с Вашия лекар или фармацевт, преди да използвате EVRA.
Болести, предавани по полов път
Това лекарство няма да ви предпази от ХИВ инфекция (СПИН) или друго полово предавано заболяване. Те включват хламидия, генитален херпес, остри брадавици, гонорея, хепатит В, сифилис. Винаги използвайте презервативи, за да се предпазите от такива заболявания.
Клинични тестове
Ако трябва да направите кръвен тест или урина, кажете на лекаря или на лицето, което събира биологичната проба, че използвате EVRA, тъй като хормоналните контрацептиви могат да повлияят на някои резултати от теста.
Деца и юноши
EVRA не е изследван при деца и юноши под 18 години. EVRA не трябва да се използва при деца и юноши, които все още не са имали първата менструация.
Взаимодействия Какви лекарства или храни могат да променят ефекта на Evra
Уведомете Вашия лекар или фармацевт, ако приемате, наскоро сте приемали или е възможно да използвате други лекарства.
Някои лекарства и билкови лекарства могат да повлияят на ефективността на EVRA.В този случай може да забременеете.
Уведомете Вашия лекар, ако приемате:
- някои антиретровирусни лекарства, използвани за лечение на ХИВ / СПИН (като нелфинавир, ритонавир, невирапин, ефавиренц)
- лекарства, използвани за лечение на инфекции (като рифампицин, рифабутин и гризеофулвин, пеницилини и тетрациклини)
- лекарства за лечение на гърчове (някои примери включват топирамат, фенорбарбитал, фенитоин, карбамазепин, примидон, оксикарбазепин, фелбамат, еликарбазепинов ацетат и руфинамид)
- фосапрепитант (лекарство за лечение на гадене)
- бозентан (лекарство за лечение на високо кръвно налягане в белодробните артерии)
- Жълт кантарион (жълт кантарион) (билково лекарство, използвано за депресия). Жълт кантарион не трябва да се приема при използване на EVRA.
Ако приемате някое от тези лекарства, трябва да използвате и допълнителен метод на контрацепция (например презерватив, диафрагма или спермицидна пяна). Интерфериращият ефект на някои от тези лекарства може да продължи до 28 дни след като сте спрели приема им. Попитайте Вашия лекар или фармацевт за друг метод на контрацепция, ако използвате EVRA едновременно с някое от изброените по -горе лекарства.
EVRA може да намали ефекта на някои лекарства като:
- лекарства, съдържащи циклоспорин
- ламотрижин, лекарство, използвано за епилепсия - това може да увеличи риска от припадъци (конвулсии)
Може да се наложи Вашият лекар да коригира дозата на други лекарства.Попитайте Вашия лекар или фармацевт за съвет, преди да приемете каквото и да е лекарство.
Предупреждения Важно е да знаете, че:
Бременност и кърмене
- Не използвайте това лекарство, ако сте бременна или мислите, че сте бременна
- Спрете да използвате това лекарство веднага, ако забременеете
- Не използвайте това лекарство, ако кърмите или планирате да кърмите
Ако сте бременна или планирате да забременеете, посъветвайте се с Вашия лекар или фармацевт, преди да приемете това лекарство.
Шофиране и работа с машини
Можете да шофирате и да работите с машини, докато използвате това лекарство.
Рискове, свързани с употребата на комбинирани хормонални контрацептиви
Следващата информация се основава на информацията относно комбинираните контрацептивни хапчета. Тъй като трансдермалният пластир EVRA съдържа хормони, подобни на тези, използвани в комбинираните контрацептивни хапчета, е вероятно да има същите рискове. Всички комбинирани противозачатъчни хапчета имат риск, който може да причини увреждане или смърт.
Трансдермален пластир като EVRA не е доказано по -безопасен от комбинираното хормонално контрацептивно хапче, приемано през устата.
Комбинирани хормонални контрацептиви и рак
Рак на шийката на матката
Ракът на маточната шийка се среща по -често при жени, приемащи комбинирани хормонални контрацептиви. Това обаче може да се дължи на други причини, включително болести, предавани по полов път.
Рак на гърдата
Наблюдавано е, че жените, които използват комбинирани хормонални контрацептиви, развиват рак на гърдата по -често от тези, които не го правят. Възможно е обаче комбинираният хормонален контрацептив да не е причина за това. Възможно е жените, приемащи комбинирани хормонални контрацептиви, да посещават по -често лекаря си. Това може да означава, че има повече шансове за диагностициране на рак на гърдата.Повишеният риск от рак на гърдата постепенно намалява след спиране на употребата на комбинирани хормонални контрацептиви. След десет години шансовете за рак на гърдата са равни на тези на жените, които никога не са използвали комбинирани хормонални контрацептиви.
Рак на черния дроб
Рядко са съобщени неракови случаи и, още по-рядко, ракови случаи на чернодробни тумори при жени, използващи комбинирани хормонални контрацептиви. Този вид тумор може да причини вътрешно кървене със силна коремна болка. Ако това се случи, незабавно се свържете с Вашия лекар.
Доза, метод и време на приложение Как да използвате Evra: Дозировка
Винаги използвайте това лекарство точно както Ви е казал Вашият лекар или фармацевт.
Ако не го направи, тя може да е изложена на по -висок риск от забременяване
Ако не сте сигурни, консултирайте се с Вашия лекар или фармацевт
Съхранявайте други нехормонални контрацептиви (като презервативи, пяна или спермицидни гъби) като резервни методи, в случай че допуснете грешки, докато използвате пластира.
Колко пластири да използвате
Седмици 1, 2 и 3: Нанесете само един пластир и го задръжте точно седем дни
седмица 4: не използвайте пластира тази седмица.
Ако през предходния цикъл не сте използвали хормонални контрацептиви
Можете да започнете това лекарство в първия ден от следващия цикъл.
Ако са изминали един или повече дни от началото на менструацията, говорете с Вашия лекар за временната употреба на нехормонални контрацептиви.
Ако преминете от оралните контрацептиви на EVRA
Ако преминавате от орални контрацептиви на EVRA:
- изчакайте менструацията
- поставете първия пластир през първите 24 часа от менструацията.
Ако пластирът е поставен след ден 1 от менструацията:
Вие също използвате нехормонални контрацептиви до 8-ия ден, когато сменяте пластира си. Ако менструацията ви не се появи в рамките на 5 дни след приемането на последното противозачатъчно хапче, говорете с Вашия лекар, преди да започнете да използвате това лекарство.
Ако преминете от прогестаген само хапче, имплант или инжекционен метод към EVRA
- Можете да започнете да приемате това лекарство всеки ден след спиране на хапчето, съдържащо само прогестоген, или деня, в който имплантът е отстранен, или в деня, предвиден за следващата инжекция.
- Поставете пластира на първия ден, след като спрете да използвате хапчета само с прогестоген, или след отстраняване на импланта, или в деня на следващата инжекция.
- Използвайте също нехормонални контрацептиви до Ден 8, когато сменяте пластира.
След спонтанен аборт или предизвикан аборт преди 20 седмици от бременността
- Говорете с Вашия лекар
- Можете да започнете незабавно това лекарство
Ако са минали един или повече дни от спонтанен аборт или предизвикан аборт, когато започнете да приемате това лекарство, говорете с Вашия лекар за временната употреба на нехормонални контрацептиви.
След спонтанен аборт или предизвикан аборт след 20 седмици от бременността
- Говорете с Вашия лекар
- Може да решите да започнете това лекарство на 21 -ия ден след предизвикан аборт или спонтанен аборт, или на първия ден от менструацията, което от двете настъпи първо.
След раждането
- Говорете с Вашия лекар
- Ако сте имали бебе и не кърмите, не трябва да използвате това лекарство четири седмици след раждането
- Ако започне повече от четири седмици след раждането, използвайте друг нехормонален контрацептив в допълнение към това лекарство през първите 7 дни
- Ако сте правили секс след раждане, изчакайте първата си менструация или се консултирайте с Вашия лекар, за да се уверите, че не сте бременна, преди да започнете да приемате това лекарство
Ако кърмите
- Говорете с Вашия лекар
- Не използвайте това лекарство, ако кърмите (вж. Точка 2 бременност и кърмене).
Важна информация, която трябва да имате предвид, когато използвате пластира
- Сменяте EVRA на същия ден всяка седмица. Пластирът е формулиран да работи в продължение на 7 дни
- Никога не позволявайте да минат повече от 7 последователни дни, без да използвате пластира
- Използвайте само един пластир наведнъж
- Не режете и не подправяйте пластира по никакъв начин
- Избягвайте поставянето на пластира върху кожа, която е зачервена, раздразнена или има порязвания
- Пластирът трябва да прилепне напълно към кожата, за да работи правилно
- Натиснете пластира здраво, докато ръбовете му се прилепнат добре
- Не използвайте кремове, масла, лосиони, талк или грим върху кожата, където поставяте пластира, или близо до пластира, който сте поставили. Това всъщност може да доведе до отлепване на пластира
- Не поставяйте нов пластир върху същата област на кожата като пластира, който току -що сте свалили. В противен случай ще има по -голям шанс за раздразнение.
- Проверявайте всеки ден, за да се уверите, че пластирът не е свален.
- Не спирайте да използвате пластирите, дори ако правите секс рядко.
КАК ДА ИЗПОЛЗВАТЕ ПАЧА
Ако използвате EVRA за първи път, изчакайте, докато получите менструация.
- Поставете първия пластир през първите 24 часа от менструацията
- Ако пластирът е поставен след Ден 1 на Вашия цикъл, ще трябва да използвате нехормонален метод за контрацепция до Ден 8, когато смените пластира.
- Денят, в който приложите първия си пластир, ще бъде Ден 1. След това „Денят за смяна на пластира“ ще бъде същия ден, всяка седмица.
Изберете място на тялото си, на което да поставите пластира.
- Винаги поставяйте пластира върху чиста, суха и обезкосмена кожа
- Нанесете пластира върху седалището, корема, външната част на горната част на ръката или горната част на гърба, където няма да се търка от тесни дрехи.
- Никога не поставяйте пластира върху гърдите си.
С пръсти отворете сашето от фолио.
- Отворете го, като го разкъсате по ръба (не използвайте ножици)
- Сега вземете здраво единия ъгъл на пластира и го извадете внимателно от сашето
- Понякога пластирите могат да залепнат във вътрешността на сашето: внимавайте да не отлепите случайно залепващото фолио, докато премахвате пластира
- Сега, както е показано на фигурата, отлепете половината от прозрачния защитен филм.
- Избягвайте да докосвате лепилната повърхност.
- Поставете пластира върху кожата.
- Едва след това отлепете другата половина на защитното фолио
- Натиснете силно върху пластира с длан за 10 секунди
- Уверете се, че ръбовете плътно прилепват.
Носите пластира 7 дни (една седмица).
- На „Денят за смяна на пластира“, който е Ден 8, премахнете използвания пластир
- Веднага поставете нов пластир.
- На Ден 15 (седмица 3) премахнете използвания пластир
- Поставете нов пластир.
Като цяло има три седмици, през които пластирите се носят.
За да избегнете дразнене, не поставяйте новия пластир на точно същото място като предишния пластир.
Не използвайте никакви пластири на седмица 4 (Ден 22 до Ден 28).
- През това време трябва да имате менструация
- През тази седмица ще бъдете защитени от бременност, но само ако започнете да използвате следващия пластир навреме.
За да започнете следващия четириседмичен цикъл
- Поставете нов пластир на нормалния си „Ден за смяна на пластира“, който е ден след 28 -ия ден
- Няма значение кой ден започва или свършва менструацията.
Ако искате да промените „Деня за смяна на пластира“ с друг ден от седмицата, моля, говорете с Вашия лекар.
Трябва да завършите текущия си цикъл и да премахнете третия пластир в правилния ден. По време на седмица 4 можете да изберете нов „Ден за смяна на пластира“ и да приложите първия пластир този ден. Не трябва да ходите повече от 7 последователни дни, без да носите пластира.
Ако искате да забавите менструацията, поставете също така пластир в началото на седмица 4 (Ден 22). Може да имате зацапване или междуменструално кървене. Не носете повече от 6 последователни пластира (така че за не повече от 6 седмици). Ако носете 6 поредни пластира (т.е. в продължение на 6 последователни седмици), не поставяйте пластира от седмица 7. След 7 дни без пластира, поставете нов пластир и рестартирайте цикъла, считайки го за Ден 1. Консултирайте се с Вашия лекар, преди да вземете решение за отлагане менструацията ти.
Ежедневни дейности, докато използвате пластира
- Нормалните дейности, като къпане, душ, сауна или упражнения, не трябва да влияят върху ефективността на пластира.
- Пластирът е формулиран да остане на място по време на тези видове дейности
- Препоръчително е обаче да проверите дали пластирът не е свален след участие в тези дейности
Ако трябва да приложите пластира на ново място в ден, различен от „Деня за смяна на пластира“
Ако пластирът, който използвате, стане неудобен или предизвика дразнене:
- можете да го отлепите и да го замените с нов пластир, поставен на различно място, до следващия „Ден за смяна на пластира“
- трябва да използвате само един пластир наведнъж.
Ако ви е трудно да си спомните да смените EVRA пластира
Говорете с Вашия лекар, фармацевт или медицински специалист за това как можете да улесните смяната на пластирите или за използването на друг метод на контрацепция.
Ако пластирът се бели или е отлепил По -малко от един ден (до 24 часа):
опитайте се да го приложите незабавно или незабавно да поставите нов пластир, не се изисква допълнителен метод на контрацепция
- вече не се придържа
- той се е прикрепил към себе си или към друга повърхност
- други материали се придържат към него
- за втори път се разхлабва или отделя.
За повече от един ден (24 часа или повече) или ако не сте сигурни колко дълго:
- незабавно започнете нов четириседмичен цикъл, като приложите нов пластир
- сега ще има нов Ден 1 и нов „Ден за смяна на пластира“
- за първата седмица от новия цикъл ще трябва да използвате и нехормонален метод за контрацепция
Може да забременеете, ако не следвате тези инструкции.
Ако забравите да смените трансдермалния пластир
В началото на всеки цикъл на приложение на кръпка (седмица 1 (ден 1)):
Ако забравите да поставите пластира, може да сте изложени на особено висок риск от забременяване.
- Следователно ще трябва да използвате нехормонален метод на контрацепция в продължение на една седмица
- Приложете първия пластир от новия цикъл веднага щом си спомните
- Вече ще имате нов „Ден за смяна на кръпки“ и нов Ден 1.
В средата на цикъла на прилагане на пластира (седмица 2 или седмица 3):
Ако забравите да смените пластира за един или два дни (до 48 часа):
- поставете нов пластир веднага щом си спомните
- приложете следващия пластир на вашия обикновен „Ден за смяна на пластира“. Не е необходима допълнителна контрацепция.
За повече от два дни (48 часа или повече):
- ако забравите да смените пластира за повече от 2 дни, може да забременеете
- започнете нов четириседмичен цикъл веднага щом си спомните, прилагането на нов пластир вече ще има различен „Ден за смяна на пластира“ и нов Ден 1
- вие също ще трябва да използвате допълнителен метод за контрацепция през първата седмица от новия си цикъл.
В края на цикъла на прилагане на пластира (седмица 4):
Ако забравите да премахнете пластира:
- премахнете пластира веднага щом си спомните
- започвате следващия цикъл на нормалния си „Ден за смяна на пластира“, който е денят след 28 -ия ден.
Не е необходима допълнителна контрацепция.
Ако нямате кървене или нередовно кървене с EVRA
Това лекарство може да причини неочаквано вагинално кървене или зацапване през седмиците, когато носите пластира
- Това обикновено приключва след първите няколко цикъла
- Грешките при използването на пластирите могат да причинят зацапване или леко кървене
- Продължете да използвате това лекарство и ако кървенето продължи по -дълго от първите три цикъла, говорете с Вашия лекар или фармацевт.
Ако менструацията ви не се появи през седмицата, в която не носите EVRA (седмица 4), трябва да продължите да прилагате нов пластир в обичайния си „Ден за смяна на пластира“.
- Ако използвате това лекарство правилно и нямате менструация, това не означава непременно, че сте бременна
- Ако обаче менструацията не настъпи за два последователни цикъла, говорете с Вашия лекар или фармацевт, тъй като може да сте бременна.
Предозиране Какво да направите, ако сте приели прекалено много Evra
Ако използвате повече EVRA, отколкото трябва (повече от един пластир EVRA наведнъж)
Отстранете пластирите и незабавно се свържете с Вашия лекар. Използването на твърде много пластири може да причини:
- неразположение (гадене, повръщане)
- вагинално кървене.
Ако сте спрели приема на EVRA
Може да имате нередовен, светъл период или изобщо да няма. Това обикновено се случва през първите 3 месеца, особено ако вашите менструации не са били редовни, преди да започнете да използвате това лекарство.
Ако имате някакви допълнителни въпроси относно употребата на това лекарство, попитайте Вашия лекар, фармацевт или медицинска сестра.
Странични ефекти Какви са страничните ефекти на Evra
Както всички лекарства, EVRA може да предизвика нежелани реакции, въпреки че не всеки ги получава. Ако получите някакви нежелани реакции, особено ако са тежки или продължителни, или ако има някаква промяна в здравето Ви, която смятате, че може да се дължи на EVRA, моля уведомете Вашия лекар.
Повишен риск от образуване на кръвни съсиреци във вените (венозна тромбоемболия (ВТЕ)) или кръвни съсиреци в артериите (артериална тромбоемболия (АТЕ)) е налице при всички жени, приемащи комбинирани хормонални контрацептиви. За по -подробна информация относно различните рискове от „приемането на комбинирани хормонални контрацептиви, вижте раздел 2„ Какво трябва да знаете, преди да използвате EVRA “.
Много чести нежелани реакции (засягат повече от 1 на 10 жени):
- Главоболие
- Гадене
- Дискомфорт в гърдите.
Чести нежелани реакции (засягат по -малко от 1 на 10 жени):
- Вагинални гъбични инфекции, понякога наричани кандидоза
- Нарушения на настроението, като депресия, промени в настроението, промени в настроението, тревожност, плач
- Замайване
- Мигрена
- Болка в стомаха или подуване на стомаха
- Повръщане или диария
- Акне, обрив, сърбеж или дразнене на кожата
- Мускулни спазми
- Проблеми с гърдите като болка в гърдите, уголемяване или бучки
- Промени в характеристиките на менструално кървене, маточни спазми, болезнени периоди, вагинално течение
- Реакции на мястото на приложение като зачервяване, дразнене, сърбеж или обрив Умора или общо неразположение
- Качване на тегло.
Нечести нежелани реакции (засягат по -малко от 1 на 100 жени):
- Алергична реакция, уртикария
- Подуване поради задържане на вода
- Високи нива на мазнини в кръвта (като холестерол или триглицериди)
- Нарушения на съня (безсъние)
- Загуба на либидо
- Екзема, зачервяване на кожата
- Ненормално производство на кърма
- Предменструален синдром
- Вагинална сухота
- Други реакции на мястото на приложение на пластира
- Подуване
- Високо кръвно налягане или повишено кръвно налягане
- Повишен апетит
- Косопад
- Чувствителност към слънчева светлина.
Редки нежелани реакции (засягат по -малко от 1 на 1 000 жени):
- вредни кръвни съсиреци във вена или артерия, например: в крак или стъпало (DVT)
- в един бял дроб (PE)
- сърдечен удар
- удар
- мини-инсулт или временни симптоми, подобни на инсулт, известни като преходна исхемична атака (TIA)
- кръвни съсиреци в черния дроб, стомаха / червата, бъбреците или окото.
- Шансът за образуване на кръвен съсирек може да бъде по -висок, ако имате някакво друго състояние, което увеличава този риск
- Рак на гърдата, шийката на матката или черния дроб
- Проблеми, причинени от контакт на пластира с кожата, като обрив с мехури или язви
- Неракови (доброкачествени) тумори на гърдата или черния дроб
- Миома на матката (матка)
- Гняв или чувство на разочарование
- Повишено либидо
- Промяна на вкуса
- Проблеми с носенето на контактни лещи
- Внезапно рязко покачване на кръвното налягане (хипертонична криза)
- Възпаление на жлъчния мехур или дебелото черво
- Променени клетки в шийката на матката
- Кафяви петна или петна по лицето
- Жлъчни камъни или запушване на жлъчните пътища
- Пожълтяване на кожата и бялото на очите
- Ненормални нива на кръвната захар или инсулина
- Подуване на лицето, устата, гърлото или езика
- Обрив с болезнени червени възли по пищялите и краката
- Сърбеж
- Люспеста, лющеща се, сърбяща и зачервена кожа
- Кърменето е потиснато
- Вагинално течение
- Задържане на течности в краката
- Задържане на течности
- Подуване на ръцете, ръцете, краката или стъпалата.
Ако имате стомашно разстройство
- Количеството освободени хормони от EVRA не трябва да се повлиява от повръщане или диария
- Не е необходимо да използвате допълнителна контрацепция, ако имате стомашно разстройство.
Може да имате зацапване, леко кървене, дискомфорт в гърдите или да се почувствате зле през първите 3 цикъла. Проблемът обикновено изчезва, но ако продължава, консултирайте се с Вашия лекар или фармацевт.
Ако получите някакви нежелани реакции, говорете с Вашия лекар, фармацевт или медицинска сестра.Това включва всички възможни нежелани реакции, които не са изброени в тази листовка.
Срок на годност и задържане
Съхранявайте това лекарство на място, недостъпно за деца.
Не използвайте това лекарство след срока на годност, отбелязан върху опаковката след "Годен до:". Срокът на годност се отнася до последния ден от този месец.
Съхранявайте в оригиналната опаковка, за да предпазите пластирите от светлина и влага.
Не съхранявайте в хладилник и не замразявайте.
Използваните пластири все още съдържат активни хормони. За да се защити околната среда, те трябва да се изхвърлят внимателно. За да изхвърлите използвания пластир, трябва:
- повдигнете етикета, който да се използва за изхвърляне, разположен от външната страна на сашето
- поставете използвания пластир вътре в етикета за изхвърляне, отворете го така, че лепкавата повърхност да покрива засенчената зона
- затворете етикета, като запечатате използвания пластир вътре и го изхвърлете на място, недостъпно за деца.
Не изхвърляйте никакви лекарства през отпадъчни води или битови отпадъци. Попитайте Вашия фармацевт как да изхвърлите лекарства, които вече не използвате. Това ще помогне за опазването на околната среда.
Източник на листовката: AIFA (Италианска агенция по лекарствата). Съдържание, публикувано през януари 2016 г. Наличната информация може да не е актуална.
За да имате достъп до най-актуалната версия, препоръчително е да получите достъп до уебсайта на AIFA (Италианска агенция по лекарствата). Отказ от отговорност и полезна информация.
01.0 ИМЕ НА ЛЕКАРСТВЕНИЯ ПРОДУКТ
ЕВРА ТРАНСДЕРМАЛЕН ПЛАСТ 203 мкг / 24 ЧАСА + 33,9 мкг / 24 ЧАСА
02.0 КАЧЕСТВЕН И КОЛИЧЕСТВЕН СЪСТАВ
Всеки 20 cm2 трансдермален пластир съдържа 6 mg норелгестромин (NGMN) и 600 mcg етинилестрадиол (EE).
Всеки трансдермален пластир освобождава средно 203 mcg NGMN и 33.9 mcg EE за 24 часа. Експозицията на лекарството се характеризира по -подходящо с фармакокинетичния профил (вж. Точка 5.2).
За пълния списък на помощните вещества вижте точка 6.1.
03.0 ЛЕКАРСТВЕНА ФОРМА
Трансдермален пластир.
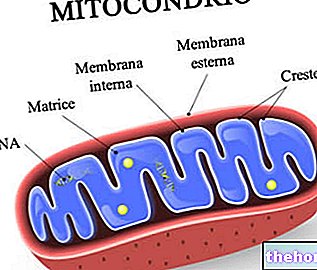
Тънък, матричен трансдермален пластир, състоящ се от три слоя.
Външната част на армиращия слой е бежов на цвят и има надпис "EVRA" термопечат.
04.0 КЛИНИЧНА ИНФОРМАЦИЯ
04.1 Терапевтични показания
Женска контрацепция.
EVRA е предназначен за жени в детеродна възраст. Ефикасността и безопасността му са установени при жени на възраст от 18 до 45 години.
Решението за предписване на EVRA трябва да вземе предвид текущите рискови фактори на отделната жена, особено тези, свързани с венозна тромбоемболия (ВТЕ), и сравнението между риска от ВТЕ, свързан с EVRA, и този, свързан с други КХК (вж. Точки 4.3 и 4.4).
04.2 Дозировка и начин на приложение
Дозировка
За да се постигне максимална контрацептивна ефикасност, информирайте пациентите, че ще трябва да използват EVRA точно както е предписано. За инструкции как да започнете, вижте „Първи стъпки с EVRA“ по -долу.
Трябва да се носи само един трансдермален пластир наведнъж.
Всеки използван трансдермален пластир трябва да бъде отстранен и незабавно заменен с нов в същия ден от седмицата (смяна на деня) на 8 и 15 ден от цикъла. Можете да смените трансдермалния пластир по всяко време на деня в деня на смяна. Четвъртата седмица, започвайки от 22 -ия ден от цикъла, трансдермалният пластир не се използва.
Нов контрацептивен цикъл започва ден след седмицата без трансдермален пластир; следващият трансдермален пластир EVRA също трябва да се постави, ако няма кървене или ако кървенето все още не е спряло.
Никога не трябва да минат повече от 7 дни без трансдермален пластир между циклите.Ако изминат повече от 7 дни, потребителят може да не бъде защитен от бременност. В този случай нехормоналната контрацепция трябва да се използва едновременно в продължение на 7 дни. Рискът от овулация се увеличава всеки ден след препоръчителния период без контрацептиви. В случай на полов акт през такъв продължителен интервал без трансдермален пластир, трябва да се има предвид възможността за бременност.
Специални популации
Телесно тегло, равно или по -голямо от 90 кг
Ефективността на контрацептивите може да бъде намалена при жени с тегло 90 kg или повече.
Бъбречна недостатъчност
EVRA не е изследван при жени с бъбречна недостатъчност.Не е необходимо коригиране на дозата, но тъй като медицинската литература предполага, че свободната фракция на етинилестрадиол е по -висока, EVRA трябва да се прилага на тази внимателно наблюдавана популация.
Чернодробна недостатъчност
EVRA не е проучен при жени с чернодробна недостатъчност. EVRA е противопоказан при жени с чернодробно увреждане (вж. Точка 4.3).
Жени след менопауза
EVRA не е показан при жени в менопауза и не трябва да се използва като хормонозаместителна терапия.
Педиатрична популация
Безопасността и ефикасността не са установени при юноши под 18-годишна възраст. Няма подходяща употреба на EVRA при деца и юноши преди менархе.
Начин на приложение
EVRA трябва да се прилага върху чиста, суха, без коса, непокътната и здрава кожа, на седалището, корема, горната външна част на ръката или горната част на торса, на място, където няма да се разтрива от тесни дрехи. EVRA не трябва да се прилага върху гърдите или кожа, която е зачервена, раздразнена или с порязвания Всеки пореден EVRA трансдермален пластир трябва да се постави върху различна част от кожата, за да се избегне дразнене, но може да остане на същата анатомична област.
Натиснете здраво върху трансдермалния пластир, докато ръбовете залепнат добре.
За да се предотврати намеса в адхезивните свойства на трансдермалния пластир, не трябва да се нанася грим, крем, лосиони, талк или други продукти за локално приложение върху областта на кожата, където е поставен трансдермалният пластир или където се предвижда да се постави. .
Препоръчва се потребителите да проверяват визуално трансдермалния пластир всеки ден, за да се гарантира правилното залепване.
Трансдермалният пластир EVRA не трябва да се реже, поврежда или променя по никакъв начин, тъй като това може да компрометира неговата контрацептивна ефикасност.
Използваните трансдермални пластири трябва внимателно да се изхвърлят съгласно инструкциите, дадени в точка 6.6.
Как да стартирате EVRA
Ако в предишния цикъл не е бил използван хормонален контрацептив
Контрацепцията с EVRA започва на първия ден от менструацията. Поставя се един трансдермален пластир и се носи цяла седмица (7 дни). Денят, в който е поставен първият трансдермален пластир (ден 1 / начален ден), определя следващите дни за подмяна. Денят за смяна на трансдермалния пластир ще бъде същия ден всяка седмица (ден 8, 15, 22 от цикъла и ден 1 от следващия цикъл). Трансдермалният пластир не се използва за четвъртата седмица, започвайки от 22 -ия ден от цикъла.
Само за първия цикъл на лечение, ако терапията от цикъл 1 започне след първия ден на менструацията, нехормоналните контрацептиви трябва да се използват едновременно през първите 7 последователни дни.
Ако преминете от комбиниран орален контрацептив
Лечението с EVRA трябва да започне в първия ден от кървенето при абстиненция. започва след първия ден на кървене при абстиненция, нехормоналните контрацептиви трябва да се използват едновременно с EVRA в продължение на 7 дни.
Ако са изминали повече от 7 дни от приемането на последното активно орално контрацептивно хапче, възможно е жената да е имала овулация. Затова Ви информираме, че трябва да се консултирате с Вашия лекар, преди да започнете лечение с EVRA. Ако жената е имала полов акт през такъв удължен интервал без хапчета, трябва да се има предвид възможността за бременност.
Ако преминете от метод само с прогестаген
Потребителят може да премине от хапче, съдържащо само прогестоген, на всеки ден (от деня на отстраняване в случай на имплант и от деня, когато трябваше да се направи инжектирането в случай на инжекционен контрацептивен метод), но през първите 7 дни ще трябва да използвате допълнителен бариерен метод на контрацепция.
След предизвикан или спонтанен аборт
След предизвикан или спонтанен аборт, настъпил преди 20 гестационна седмица, потребителят може да започне да използва EVRA незабавно. Ако EVRA се започне незабавно, не се изискват допълнителни мерки за контрацепция. Моля, обърнете внимание, че овулацията може да настъпи в рамките на 10 дни след предизвикан или спонтанен аборт. .
В случай на предизвикан или спонтанен аборт, настъпил на 20 гестационна седмица или по -късно, EVRA може да започне на 21 ден след аборта или на първия ден от първата спонтанна менструация, в зависимост от това кое от двете настъпи първо. 21 ден след аборт (на 20 гестационна седмица).
След раждането
Потребителите, които решат да не кърмят, трябва да започнат контрацептивна терапия с EVRA не по -рано от 4 седмици след раждането. С по -късно начало информирайте потребителя за необходимостта от използване на допълнителен бариерен метод през първите 7 дни, но ако полов акт вече е настъпил, изключете възможността за бременност преди започване на EVRA или изчакайте първия период.
За кърмещи жени вижте точка 4.6.
Какво да направите, ако трансдермалният пластир се отдели частично или напълно
Ако трансдермалният пластир EVRA частично или напълно се отделя и остава отделен, количеството на доставения лекарствен продукт няма да бъде достатъчно.
Ако EVRA остане дори само частично отделена:
• за по -малко от един ден (до 24 часа): трябва да се постави отново на същото място или незабавно да се замени с нов трансдермален пластир EVRA. Не са необходими други мерки за контрацепция. Поставете следващия EVRA трансдермален пластир на обичайния си „Ден за смяна“.
• за повече от един ден (24 часа или повече) или ако потребителят не знае кога трансдермалният пластир е повдигнат или отделен: потребителят може да не е защитен от бременност. Потребителят трябва да спре контрацептивния цикъл и незабавно да започне нов, като постави нов трансдермален пластир EVRA. Сега има нов „ден 1“ и нов „ден за смяна“. Нехормонален метод на контрацепция също трябва да се използва едновременно ... само за първите 7 дни от новия цикъл.
Трансдермален пластир не трябва да се поставя отново, ако вече не е залепващ, незабавно го заменете с нов. Не трябва да се използват никакви други лепила или превръзки за задържане на трансдермалния пластир EVRA на място.
В случай на забавяне в следващите дни на подмяна на EVRA трансдермални пластири
В началото на всеки цикъл с трансдермален пластир (първа седмица / ден 1):
Потребителката може да не е защитена от бременност. Тя трябва да постави първия трансдермален пластир от новия цикъл веднага щом си спомни. Вече има нов „Ден за смяна“ и нов „Ден 1“ хормонален за първите 7 дни от новият цикъл В случай на полов акт през такъв продължителен период без трансдермален пластир, трябва да се има предвид възможността за бременност.
Среден цикъл (втора седмица / ден 8 или трета седмица / ден 15):
• за един до два дни (до 48 часа): Потребителят трябва незабавно да постави нов EVRA трансдермален пластир. Следващият EVRA трансдермален пластир трябва да се постави на обичайния „ден за смяна“. Ако през 7 -те дни, предхождащи първия ден, ако трансдермалният пластир не е поставен, потребителят е носил пластира правилно, не са необходими допълнителни мерки за контрацепция.
• за повече от два дни (48 часа или повече): „Потребителката може да не е защитена от бременност. Тя трябва да спре сегашния си контрацептивен цикъл и незабавно да започне нов четириседмичен цикъл, като постави нов трансдермален пластир EVRA. Сега ще да има нов „ден 1“ и нов „ден на замяна“ .Нехормоналните контрацептиви трябва да се използват едновременно през първите 7 последователни дни от новия цикъл.
• в края на цикъла (седмица 4 / ден 22): Ако потребителят не премахне трансдермалния пластир EVRA в началото на седмица 4 (ден 22), той трябва да го отстрани възможно най -скоро. Следващият цикъл трябва да започне с нормалния "ден за подмяна", който е ден след ден 28. Не са необходими допълнителни мерки за контрацепция.
За да промените деня за смяна
Ако потребителят желае да отложи менструацията си веднъж, той трябва да постави друг трансдермален пластир в началото на седмица 4 (ден 22), като по този начин не спазва интервала без пластири. Може да имате кървене или зацапване. След носене на трансдермалния пластир в продължение на 6 последователни седмици трябва да има интервал без пластири от 7 дни, след което редовното прилагане на EVRA се възобновява.
Ако потребителят желае да промени деня на смяна, той трябва да завърши текущия цикъл, като премахне третия трансдермален пластир EVRA на правилния ден. По време на интервала без трансдермален пластир, тя може да избере нов ден за смяна, като постави първия трансдермален пластир EVRA от следващия цикъл веднага щом настъпи желаният ден. Никога повече от 7 дни не трябва да минат без трансдермалния пластир. Колкото по-кратък е интервалът без пластири, толкова по-голям е рискът потребителят да няма кървене при абстиненция и вместо това да има метрорагия и зацапване по време на следващия цикъл на лечение.
В случай на леко дразнене на кожата
Ако използването на трансдермалния пластир причинява „досадно дразнене, може да се постави нов трансдермален пластир върху друга част“ до достигане на следващия ден за подмяна. Трябва да се използва само един трансдермален пластир наведнъж.
04.3 Противопоказания
Комбинирани хормонални контрацептиви (комбинирани хормонални контрацептиви, COC) не трябва да се използва при следните условия. Ако някой от тези симптоми се появи по време на употреба на EVRA, незабавно преустановете употребата.
• Наличие или риск от венозна тромбоемболия (ВТЕ)
• Венозна тромбоемболия - текуща (с прием на антикоагуланти) или предишна ВТЕ (напр. Дълбока венозна тромбоза [DVT] или белодробна емболия [PE])
• Известна наследствена или придобита предразположеност към венозна тромбоемболия, като резистентност към активиран протеин С (включително фактор V Leiden), дефицит на антитромбин III, дефицит на протеин С, дефицит на протеин S
• Тежка операция с продължително обездвижване (вж. Точка 4.4)
• Висок риск от венозна тромбоемболия поради наличието на множество рискови фактори (вж. Точка 4.4)
• Наличие или риск от артериална тромбоемболия (ATE)
• Артериална тромбоемболия - настояща или предишна артериална тромбоемболия (напр. Миокарден инфаркт) или продромални състояния (напр. Ангина пекторис)
• Цереброваскуларно заболяване - настоящ или предишен инсулт или продромални състояния (напр. Преходна исхемична атака (преходна исхемична атака, TIA))
• Известна наследствена или придобита предразположеност към артериална тромбоемболия, като хиперхомоцистеинемия и антифосфолипидни антитела (антикардиолипинови антитела, лупусов антикоагулант)
• История на мигрена с фокални неврологични симптоми
• Висок риск от артериална тромбоемболия поради наличието на множество рискови фактори (вж. Точка 4.4) или наличието на сериозен рисков фактор като:
• захарен диабет със съдови симптоми
• тежка хипертония
• тежка дислипопротеинемия
• Свръхчувствителност към активните вещества или към някое от помощните вещества, изброени в точка 6.1.
• Известен или предполагаем рак на гърдата
• Рак на ендометриума или други известни или предполагаеми естроген-зависими неоплазми
• Променена чернодробна функция, свързана с остро или хронично хепатоцелуларно заболяване
• Чернодробни аденоми или карциноми
• Недиагностицирано анормално генитално кървене
04.4 Специални предупреждения и подходящи предпазни мерки при употреба
Предупреждения
Ако има някое от посочените по -долу състояния или рискови фактори, пригодността на EVRA трябва да се обсъди с жената.
В случай на влошаване или първа поява на някой от тези рискови фактори или състояния, жената трябва да се свърже с лекаря си, за да определи дали употребата на EVRA трябва да се преустанови.
Няма клинични доказателства, които да показват, че трансдермалният пластир е по -безопасен от КОК във всяко отношение.
EVRA не е показан при бременност (вж. Точка 4.6).
Риск от венозна тромбоемболия (ВТЕ)
Употребата на който и да е комбиниран хормонален контрацептив (КОК) води до повишен риск от венозна тромбоемболия (ВТЕ) в сравнение с липсата на употреба. Продукти, които съдържат левоноргестрел, норгестимат или норетистерон, са свързани с по -нисък риск от ВТЕ. Рискът, свързан с други. Продукти като EVRA също могат да бъдат двойни. Решението да се използва продукт, различен от тези, свързани с по -нисък риск от ВТЕ, трябва да се вземе само след разговори с жената, за да се гарантира, че тя разбира риска от ВТЕ, свързан с EVRA. фактори влияят върху този риск и факта, че рискът от развитие на ВТЕ е най -висок през първата година от употребата.Съществуват и някои доказателства, че рискът се увеличава, когато приемът на КОК се възобнови след почивка от 4 или повече седмици.
Около 2 от 10 000 жени, които не използват CHC и които не са бременни, ще развият ВТЕ за период от една година. При една жена обаче рискът може да бъде много по -висок, в зависимост от нейните основни рискови фактори (виж по -долу).
Смята се, че от 10 000 жени, които използват нискодозови CHC, съдържащи левоноргестрел, около 6 [1] ще развият ВТЕ за една година. Проучванията показват, че честотата на ВТЕ при жените, които са използвали EVRA, е до два пъти по-висока, отколкото при потребителите на КОК, които съдържат левоноргестрел. Тези стойности са приблизително 6-12 ВТЕ годишно за 10 000 жени, използващи EVRA.
[1] Средна стойност от диапазона 5-7 на 10 000 жени / година, въз основа на относителен риск от приблизително 2,3-3,6 от КОК, съдържащи левоноргестрел, в сравнение с неупотребата
И в двата случая броят на ВТЕ годишно е по -нисък от очаквания брой при бременни жени или жени след раждането.
ВТЕ може да бъде фатално в 1-2% от случаите.
Много рядко се съобщава за тромбоза при потребители на CHC в други кръвоносни съдове, например чернодробни, мезентериални, бъбречни или ретинални вени и артерии.
Рискови фактори за ВТЕ
Рискът от венозни тромбоемболични усложнения при потребителите на КХК може да се увеличи значително, ако са налице допълнителни рискови фактори, особено ако има повече от един рисков фактор (вж. Таблицата).
EVRA е противопоказан, ако жената има множество рискови фактори, които увеличават риска от венозна тромбоза (вж. Точка 4.3). Ако една жена има повече от един рисков фактор, възможно е повишеният риск да е по-голям от сумата на отделните фактори; в този случай трябва да се вземе предвид общият й риск от ВТЕ. Ако съотношението полза-риск се счита за отрицателно , не трябва да се предписва СНС (вж. точка 4.3).
Таблица: Рискови фактори за ВТЕ
Няма съгласие относно възможната роля на разширените вени и повърхностния тромбофлебит в началото и прогресията на венозна тромбоза.
Трябва да се има предвид повишеният риск от тромбоемболия по време на бременност, особено 6-седмичния период на пуерпериума (за информация относно "Бременност и кърмене" вижте точка 4.6.
Симптоми на ВТЕ (дълбока венозна тромбоза и белодробна емболия)
Ако се появят симптоми от този тип, жените трябва незабавно да потърсят медицинска помощ и да ги информират, че приемат ХСГ.
Симптомите на дълбока венозна тромбоза (ДВТ) могат да включват:
• едностранно подуване на крака и / или стъпалото или по протежение на вена в крака;
• болка или нежност в крака, които могат да се усетят само при изправяне или ходене;
• повишено усещане за топлина в засегнатия крак; кожа на крака, която е червена или обезцветена.
Симптомите на белодробна емболия (РЕ) могат да включват:
• внезапно и необяснимо начало на задух и учестено дишане;
• внезапна кашлица, която може да бъде свързана с хемоптиза;
• остра болка в гърдите;
• силно замаяност или замаяност;
• ускорен или неравномерен сърдечен ритъм.
Някои от тези симптоми (като „задух“ и „кашлица“) са неспецифични и могат да бъдат тълкувани погрешно като по-чести или по-малко сериозни събития (например инфекции на дихателните пътища).
Други признаци на съдова оклузия могат да включват: внезапна болка, подуване или бледосиньо обезцветяване на един „крайник.
Ако оклузията се осъществи в окото, симптомите могат да варират от безболезнено замъгляване на зрението до загуба на зрение. Понякога загубата на зрение се случва почти веднага.
Риск от артериална тромбоемболия (ATE)
Епидемиологичните проучвания свързват употребата на ХСС с повишен риск от артериална тромбоемболия (инфаркт на миокарда) или от мозъчно -съдови инциденти (напр. Преходна исхемична атака, инсулт). Артериалните тромбоемболични събития могат да бъдат фатални.
Рискови фактори за ATE
Рискът от артериални тромбоемболични усложнения или мозъчно -съдов инцидент при потребителите на CHC се увеличава при наличието на рискови фактори (вж. Таблицата). EVRA е противопоказан, ако жената има един сериозен рисков фактор или множество рискови фактори за АТЕ, които увеличават риска от артериална тромбоза (вж. Точка 4.3). Ако една жена има повече от един рисков фактор, възможно е увеличаването на риска да е по-голямо от сумата на отделните фактори; в този случай трябва да се вземе предвид общият й риск. Ако се смята, че балансът полза-риск е отрицателен, не трябва да се предписва СНС (вж. точка 4.3).
Таблица: Рискови фактори за ATE
Симптоми на ATE
Ако се появят симптоми от този тип, жените трябва незабавно да се свържат с медицински специалист и да ги информират, че приемат ХСК.
Симптомите на мозъчно -съдов инцидент могат да включват:
• внезапно изтръпване или слабост на лицето, ръката или крака, особено от едната страна на тялото;
• внезапно затруднено ходене, виене на свят, загуба на равновесие или координация;
• внезапно объркване, трудности при говорене или разбиране;
• внезапно затруднено виждане на едното или на двете очи;
• внезапна, тежка или продължителна мигрена без известна причина;
• загуба на съзнание или припадък със или без конвулсии.
Временните симптоми предполагат, че това е преходна исхемична атака (TIA).
Симптомите на миокарден инфаркт могат да включват:
• болка, дискомфорт, натиск, тежест, усещане за притискане или пълнота в гърдите, ръката или под гръдната кост;
• дискомфорт, излъчващ към гърба, челюстта, гърлото, ръцете, стомаха;
• чувство на ситост, лошо храносмилане или задушаване;
• изпотяване, гадене, повръщане или замаяност;
• крайна слабост, безпокойство или задух;
• бърз или неравномерен сърдечен ритъм.
Жените, използващи комбинирани контрацептиви, трябва да се свържат с лекаря си в случай на възможни симптоми на тромбоза.Ако има съмнение или е известна тромбоза, прекратете употребата на хормонални контрацептиви. Започнете адекватна контрацепция поради тератогенността на антикоагулантната терапия (кумарини).
Тумори
В някои епидемиологични проучвания се съобщава за повишен риск от рак на шийката на матката при дългосрочни потребители на КОК, но степента, до която тази находка може да се дължи на объркващия ефект на сексуалното поведение и други фактори като човешки папиломен вирус, продължава да бъде противоречива (HPV ).
Мета-анализ на 54 епидемиологични проучвания съобщава за малко по-висок риск (RR = 1,24) от диагнозата рак на гърдата при жени, които в момента използват КОК. Излишният риск постепенно изчезва през 10 -те години след прекратяването на употребата на КОК. Тъй като ракът на гърдата е рядък при жени под 40 години, по -големият брой диагностицирани ракови заболявания на гърдата сред настоящите потребители и последните КОК е ограничен по отношение на общия риск от рак на гърдата. Ракът на гърдата, диагностициран при жени, които са използвали КОК, има тенденция да бъде по -слабо клинично напреднал от рака, открит при жени, които никога не са приемали КОК.Наблюдаваният модел на по -висок риск може да се дължи на ранна диагностика на рак на гърдата при употребяващи КОК, биологичните ефекти на КОК или комбинация от двете.
В редки случаи сред употребяващите КОК са докладвани доброкачествени чернодробни тумори, а при още по -редки - злокачествени чернодробни тумори. В единични случаи, тези тумори са довели до животозастрашаващи интраабдоминални кръвоизливи. Следователно, помислете за възможността за рак на черния дроб при диференциалната диагноза, когато потребителят на EVRA има тежка болка в горната част на корема, уголемяване на черния дроб или признаци на интраабдоминален кръвоизлив.
Други условия
• Ефикасността на контрацептивите може да бъде намалена при жени с тегло 90 kg или повече (вж. Точки 4.2 и 5.1).
• Жените с хипертриглицеридемия или фамилна анамнеза за нея могат да бъдат изложени на повишен риск от панкреатит, докато използват комбинирани хормонални контрацептиви.
• Въпреки че се съобщава за малко повишаване на кръвното налягане при много жени, приемащи хормонални контрацептиви, клинично значимите повишения са редки. Определена връзка между употребата на хормонални контрацептиви и клиничната хипертония не е установена. Ако по време на употребата на комбиниран хормонален контрацептив в присъствието на съществуваща хипертония, постоянно високото кръвно налягане или значително повишаване на кръвното налягане не реагира адекватно на антихипертензивно лечение, прекратете употребата на комбиниран хормонален контрацептив. Тази употреба може да бъде възобновена, ако е възможно да се получат нормотензивни стойности чрез антихипертензивна терапия.
• Появата или влошаването на следните състояния е докладвана както при бременността, така и при употребата на КОК. Въпреки това, доказателствата за връзка с употребата на КОК не са убедителни: жълтеница и / или пруритус, свързани с холестаза; заболяване на жлъчния мехур, включително холецистит и холелитиаза; порфирия; системен лупус еритематозус; хемолитично -уремичен синдром; хорея на Sydenham; гестационен херпес; загуба на слуха, свързана с отосклероза.
• Остри или хронични нарушения на чернодробната функция може да наложат прекъсване на комбинираните хормонални контрацептиви, докато маркерите на чернодробната функция се върнат към нормалните си стойности.налагат прекратяване на комбинираните хормонални контрацептиви.
• Въпреки че комбинираните хормонални контрацептиви могат да имат ефект върху периферната инсулинова резистентност и глюкозния толеранс, няма доказателства, че схемата на лечение трябва да бъде променена при пациенти с диабет, докато се използва комбинирана хормонална контрацепция. Жените с диабет обаче трябва да се наблюдават внимателно, особено в ранните етапи на използване на EVRA.
• Съобщава се за влошаване на ендогенна депресия, епилепсия, болест на Crohn и улцерозен колит по време на употребата на КОК.
• Понякога хлоазма може да възникне при употребата на хормонална контрацепция, особено при потребители с анамнеза за хлоазма гравидарум Потребителите с тенденция към хлоазма трябва да избягват излагане на слънце или ултравиолетова радиация, докато използват EVRA. Хлоазмата често не е напълно обратима.
Медицински прегледи / посещения
Преди започване или възобновяване на употребата на EVRA трябва да се вземе пълна анамнеза (включително фамилна анамнеза) и да се изключи бременността. Трябва да се измери кръвното налягане и да се извърши клиничен преглед, ръководен от противопоказания (вж. Точка 4.3) и предупреждения (вж. точка 4.4). Важно е да се привлече вниманието на жената към информация, свързана с венозна или артериална тромбоза, включително риска, свързан с EVRA в сравнение с други КХК, симптоми на ВТЕ и АТЕ, известни рискови фактори и какво да се прави в случай съмнение за тромбоза.
Жената също трябва да бъде уведомена за необходимостта да прочете внимателно листовката и да следва съветите й. Честотата и видът на прегледите трябва да се основават на установените насоки и да бъдат адаптирани към индивидуалната жена.
Жените трябва да бъдат предупредени, че оралните контрацептиви не предпазват от ХИВ инфекции (СПИН) и други болести, предавани по полов път.
Нередовно кървене
Както при всички комбинирани хормонални контрацептиви, може да възникне нередовна загуба на кръв (зацапване или пробивно кървене), особено през първите месеци на употреба. Поради тази причина медицинското мнение за нередовна загуба на кръв ще бъде полезно само след период на корекция от приблизително три цикъла. Трябва да се има предвид EVRA. Помислете за нехормонални причини и, ако е необходимо, вземете подходящи диагностични мерки, за да изключите наличието на органично заболяване или бременност. Тези мерки могат да включват кюретаж. При някои жени може да няма кървене от суспензия в интервал на използване на трансдермалния пластир. Ако EVRA е била взета съгласно инструкциите в точка 4.2, е малко вероятно жената да е бременна. Ако обаче EVRA не е била взета съгласно тези инструкции преди първото пропуснато кървене при оттегляне или ако жената е пропуснала две последователни кървения при оттегляне, бременността трябва да се изключи, преди да продължи да използва EVRA.
Някои потребители може да имат аменорея или олигоменорея след спиране на хормоналната контрацепция, особено ако тези състояния са съществували преди това.
04.5 Взаимодействия с други лекарствени продукти и други форми на взаимодействие
Забележка: Консултирайте се с информацията за предписване на съпътстващи лекарства, за да идентифицирате възможните взаимодействия.
Влияние на други лекарствени продукти върху EVRA
Взаимодействието между орални контрацептиви и други лекарства може да доведе до загуба на кръв и / или неуспех на контрацептивната защита. В литературата са съобщени следните взаимодействия.
Чернодробен метаболизъм
Могат да се наблюдават взаимодействия с лекарства, индуциращи чернодробни ензими, които могат да доведат до повишен клирънс на половите хормони (например фенобарбитал, примидон, рифампицин, рифабутин, бозентан, (фос) апрепитант), някои антиепилептици (напр. Карбамазепин), есликарбазепинов ацетат, фелбамат , оксикарбазепин, фенитоин, руфинамид, топирамат) и някои лекарства за лечение на ХИВ (напр. нелфинавир, ритонавир, невирапин, ефавиренц) и евентуално също гризеофулвин и продукти, съдържащи жълт кантарион (Hypericum perforatum). Максималната ензимна индукция обикновено настъпва след около 10 дни, но може да се поддържа поне 4 седмици след прекратяване на терапията.
Не използвайте билкови препарати, съдържащи жълт кантарион (Hypericum perforatum)), докато използвате EVRA.
Интерференция с ентерохепаталния кръг
Съобщавани са и случаи на неуспешна контрацепция с антибиотици като пеницилини и тетрациклини. Механизмът на този ефект все още не е ясен. В проучване за фармакокинетично взаимодействие, пероралното приложение на тетрациклин хидрохлорид, 500 mg четири пъти дневно в продължение на 3 дни преди периода на приложение на EVRA и в продължение на 7 дни през този период, не повлиява значително фармакокинетиката на норелгестромин или етинил естрадиол.
Управление
Жените на краткосрочно лечение с някой от лекарствените продукти, принадлежащи към един от горните класове, или с активни вещества, които индуцират чернодробни ензими (с изключение на рифампицин), трябва временно да използват бариерен метод в допълнение към EVRA, т.е. по време на периода на едновременна употреба от тези лекарства и 7 дни след прекратяването им. За жени, лекувани с рифампицин, трябва да се използва бариерен метод в допълнение към EVRA заедно с периода на рифампицин и в продължение на 28 дни след прекратяването му.
За жени на продължителна терапия с някое от лекарствата, принадлежащи към един от горните класове, се препоръчва да се използва друг ефективен нехормонален метод на контрацепция.
Жените, лекувани с антибиотици (с изключение на рифампицин, вижте по -горе), ще трябва да използват бариерен метод до 7 дни след спиране на лекарството.
Ако съпътстващото лечение продължава след края на седмицата за лечение с пластира, новият пластир трябва да се приложи незабавно, като се започне нов курс на лечение, без да се спазва обичайният интервал без пластири.
Инхибиране на метаболизма на етинилестрадиола
Доказано е, че еторикоксиб повишава плазмените нива на етинилестрадиол (50 до 60%), когато се приема едновременно с трифазен перорален хормонален контрацептив. Смята се, че еторикоксиб повишава нивата на етинилестрадиол чрез инхибиране на активността на сулфотрансферазата, като по този начин инхибира метаболизма на етинилестрадиола.
Влияние на EVRA върху други лекарствени продукти
Хормоналните контрацептиви могат да повлияят на метаболизма на някои активни съставки. Следователно плазмените и тъканните концентрации могат да се увеличат (например циклоспорин). Може да се наложи коригиране на дозата на съпътстващото лекарство.
Ламотрижин: Комбинираните хормонални контрацептиви показват значително намаляване на плазмените концентрации на ламотрижин при едновременно приложение, вероятно поради индуциране на глюмониране на ламотрижин.
Лабораторен тест
Използването на стероидни хормони с контрацептивно действие може да повлияе на резултатите от някои лабораторни тестове, включително биохимични параметри, свързани с чернодробната, щитовидната, надбъбречната и бъбречната функция, плазмените нива на протеини (носители), като например кръвосвързващи глобулинови кортикостероиди и липидни / липопротеинови фракции, параметри на въглехидратния метаболизъм и параметри на коагулация и фибринолиза Вариациите обикновено остават в рамките на нормалните лабораторни граници.
04.6 Бременност и кърмене
Бременност
EVRA не е показан по време на бременност.
Епидемиологичните проучвания показват, че няма по -голям риск от вродени дефекти при деца, родени от жени, които са използвали КОК преди бременността. Освен това, последните проучвания не показват тератогенен ефект, когато КОК се използват по невнимание през ранните етапи на бременността.
Ограничените налични данни за резултатите от експозиция на бременност при жени, лекувани с EVRA, не позволяват заключения относно безопасността на трансдермалния пластир по време на бременност.
Проучванията при животни показват нежелани ефекти по време на бременност и кърмене (вж. Точка 5.3). Въз основа на тези данни при животни нежеланите ефекти, дължащи се на хормоналното действие на активните съединения, не могат да бъдат изключени. Въпреки това, общият опит с КОК по време на бременност не дава доказателства за реален неблагоприятен ефект при хора.
Ако забременеете, докато приемате EVRA, незабавно спрете употребата на EVRA.
Повишеният риск от ВТЕ по време на следродилния период трябва да се има предвид при възобновяване на EVRA (вж. Точки 4.2 и 4.4).
Време за хранене
Кърменето може да бъде повлияно от комбинирани хормонални контрацептиви, тъй като те могат да намалят обема и да променят състава на кърмата.Поради това употребата на EVRA не се препоръчва при майки, които кърмят, докато бебето не се отбие напълно.
Плодовитост
При жените може да има забавяне на зачеването след спиране на EVRA.
04.7 Ефекти върху способността за шофиране и работа с машини
EVRA няма или има незначително влияние върху способността за шофиране или работа с машини.
04.8 Нежелани реакции
Обобщение на профила на безопасност
Най -често съобщаваните нежелани реакции в клиничните изпитвания са главоболие, гадене и дискомфорт в гърдите и се наблюдават съответно при приблизително 21,0%, 16,6% и 15,9% от жените.
Нежеланите реакции, които могат да се появят в началото на лечението, но обикновено отшумяват след първите три курса, включват кървене, дискомфорт в гърдите и гадене.
Описание на някои нежелани реакции
Повишен риск от артериални и венозни тромботични и тромбоемболични събития, включително инфаркт на миокарда, инсулт, преходни исхемични атаки, венозна тромбоза и белодробна емболия, е наблюдаван при потребители на КХК и този риск е обсъден по -подробно в точка 4.4.
Таблица със списък на нежеланите реакции
Безопасността е оценена при 3 322 сексуално активни жени, които са участвали в три клинични изпитвания фаза III, предназначени да оценят ефикасността на контрацептивите. Тези пациенти са получили шест или 13 цикъла на контрацепция (EVRA или орален контрацептив като сравнител)., Са взели поне една доза проучване лекарствен продукт и предоставени данни за безопасност. Таблица 1 по-долу отразява нежеланите реакции, съобщени в клинични изпитвания и постмаркетинговия опит. Конвенция за честотата на MedDRA: много често (≥ 1/10); чести (≥ 1/100 г.
04.9 Предозиране
Не са докладвани сериозни странични ефекти след случайно поглъщане на големи количества орални контрацептиви. Предозирането може да причини гадене и повръщане. Някои жени могат да получат вагинално кървене.
05.0 ФАРМАКОЛОГИЧНИ СВОЙСТВА
05.1 Фармакодинамични свойства
Фармакотерапевтична група: Полови хормони и модулатори на гениталната система, прогестагени и естрогени, фиксирана асоциация. ATC код: G03AA13.
Механизъм на действие
EVRA действа чрез механизма на потискане на гонадотропина чрез естрогенното и прогестиновото действие на етинилестрадиол и норелгестромин. Основният механизъм на действие е инхибирането на овулацията, но също така промените в цервикалната слуз и ендометриума могат да допринесат за ефикасността на продукта.
Клинична ефикасност и безопасност
Перлени индекси (виж таблицата):
*: DSG 150 mcg + 20 mcg EE
**: 50 mcg LNG +30 mcg EE за дни 1-6, 75 mcg LNG + 40 mcg EE за дни 7-11, 125 mcg LNG + 30 mcg EE за дни 12-21
Бяха извършени проучвателни анализи, за да се определи дали в проучванията фаза III (n = 3319) характеристиките на популацията, като възраст, раса и тегло, могат да бъдат свързани с бременността. Анализите не показват никаква връзка между възрастта и расата с бременността, но по тегло 5 от 15 -те бременности, съобщени с EVRA, са били при жени с телесно тегло равно или по -голямо от 90 kg в началото, което представлява
С използването на по-високи дози КОК (50 мкг етинилестрадиол) се намалява рискът от рак на ендометриума и яйчниците. Остава да се потвърди дали това се отнася и за по-ниски дози комбинирани хормонални контрацептиви.
05.2 Фармакокинетични свойства
Абсорбция
След прилагане на EVRA, серумните нива на норелгестромин и етинил естрадиол достигат плато в рамките на приблизително 48 часа. стабилно състояние на норелгестромин и ЕЕ по време на една седмица от използването на трансдермалния пластир са приблизително 0,8 ng / mL и 50 pg / mL, съответно. до седмица 1 на цикъл 1.
Абсорбцията на норелгестромин и етинил естрадиол след прилагане на EVRA е изследвана при условията, открити във фитнес залата (сауна, джакузи, бягаща пътека и други аеробни упражнения) и в баня със студена вода. Резултатите показват, че за норелгестромин няма значителни ефекти от лечението на CSS или AUC в сравнение с нормалната употреба. За ЕЕ се наблюдава леко увеличение от бягащата пътека и други аеробни упражнения, но стойностите на CSS след тези лечения останаха в референтния диапазон. Нямаше значителен ефект на студената вода върху тези параметри.
Резултатите от проучване с EVRA за продължителна употреба на единичен трансдермален пластир за 7 дни и 10 дни показват, че целевият CSS за норелгестромин и етинил естрадиол се поддържа в продължение на 3-дневно удължаване на употребата на EVRA. (10 дни) Тези резултати предполагат, че клиничната ефикасност трябва да се поддържа, дори ако пластирът е забравен за до 2 пълни дни.
Разпределение
Норелгестромин и норгестрел (серумен метаболит на норелгестромин) са силно свързани (> 97%) със серумните протеини. Норелгестроминът е свързан с албумин, а не с SHBG, докато норгестрел е свързан главно с SHBG, което ограничава неговата биологична активност. Етинилестрадиолът е силно свързан със серумния албумин.
Биотрансформация
Норелгестроминът се метаболизира от черния дроб и метаболитите включват норгестрел, който се свързва в голяма степен с SHGB, и различни хидроксилирани и конюгирани метаболити. Етинилестрадиолът също се метаболизира до различни хидроксилирани продукти и техните конюгати с глюкурониди и сулфати.
Елиминиране
След отстраняване на трансдермалния пластир, елиминационният полуживот на норелгестромин и етинил естрадиол е съответно приблизително 28 часа и 17 часа. Метаболитите на норелгестромин и етинил естрадиол се елиминират чрез бъбреците и изпражненията.
Трансдермални контрацептиви срещу орални контрацептиви
Фармакокинетичните профили на комбинираните трансдермални и перорални хормонални контрацептиви са различни и трябва да се внимава, когато се прави директно сравнение между фармакокинетичните параметри на тези две формулировки.
В проучване, сравняващо EVRA с орален контрацептив, съдържащ норгестимат (предшественик на норелгестромин) 250 mcg / етинил естрадиол 35 mcg, стойностите на Cmax са 2 пъти по-високи за норелгестромин и етинил естрадиол при лица, на които е прилаган перорален контрацептив в сравнение с EVRA, докато общата експозиция (AUC и Css) е сравнима с тази на субектите, лекувани с EVRA.
Междуиндивидуалната вариабилност (% CV) във фармакокинетичните параметри на EVRA е по-голяма от тази, наблюдавана при перорални контрацептиви.
Ефекти от възрастта, телесното тегло и телесната повърхност
Ефектите от възрастта, телесното тегло и телесната повърхност върху фармакокинетиката на норелгестромин и етинил естрадиол са оценени при 230 здрави жени в девет фармакокинетични проучвания с еднократно приложение на EVRA в продължение на 7 дни. Увеличаването на възрастта, теглото и телесната повърхност са свързани с леко намаляване на стойностите на Css и AUC както за норелгестромин, така и за ЕЕ.Но само малък процент (10-20%) от общата променливост във фармакокинетиката на норелгестромин и ЕЕ след прилагане на EVRA може да бъде свързан с някои или всички от горните демографски параметри.
05.3 Предклинични данни за безопасност
Неклиничните данни не разкриват особен риск за хората въз основа на конвенционални проучвания за фармакология за безопасност, токсичност при многократни дози, генотоксичност и канцерогенен потенциал. По отношение на репродуктивната токсичност, норелгестроминът демонстрира фетална токсичност при зайци, но границата на безопасност за този ефект е достатъчно висока. Няма данни за репродуктивната токсичност на комбинацията от норелгестромин с етинил естрадиол.Данните за комбинацията от норгестимат (предшественик на норелгестромин) с етинил естрадиол показват намаляване на плодовитостта и ефикасността при женски животни. Имплантиране (плъхове), увеличение при фетална резорбция (плъхове, зайци) и при високи дози намаляване на жизнеспособността и плодовитостта на женските раждания (плъхове).Значението на тези данни за експозицията при хора не е известно, тъй като се счита, че ефектите са свързани с фармакодинамични действия или специфични действия за тези животински видове с вече известен характер.
Проучванията, проведени за изследване на дермалните ефекти на EVRA, показват, че тази система няма потенциал да предизвика сенсибилизация и може да предизвика само леко дразнене, когато се прилага върху заешка кожа.
06.0 ФАРМАЦЕВТИЧНА ИНФОРМАЦИЯ
06.1 Помощни вещества
Подсилващ слой
външен слой от пигментиран полиетилен с ниска плътност, вътрешен слой от полиестер.
Междинен слой
полиизобутилен / адхезивен полибутен, кросповидон, нетъкан полиестер, лаурил лактат.
Трети слой
полиетилен терефталатен (PET) филм, полидиметилсилоксаново покритие.
06.2 Несъвместимост
Не е от значение.
06.3 Срок на валидност
2 години.
06.4 Специални условия на съхранение
Съхранявайте в оригиналната опаковка, за да предпазите пластирите от светлина и влага.
Не съхранявайте в хладилник и не замразявайте.
06.5 Естество на непосредствената опаковка и съдържанието на опаковката
Първичен опаковъчен материал
Всяко саше се състои от четири слоя: полиетиленов филм с ниска плътност (най -вътрешният слой), алуминиево фолио, полиетиленов филм с ниска плътност и външен слой от избелена хартия.
Вторичен опаковъчен материал
Сашетата са опаковани в картонена кутия.
Всяка опаковка съдържа 3, 9 или 18 EVRA трансдермални пластира в отделни подсилени сашета.
Сашетата са опаковани, на три групи, в прозрачен перфориран пластмасов филм и опаковани в картонена кутия.
Не всички опаковки могат да бъдат пуснати на пазара.
06.6 Инструкции за употреба и боравене
Пластирът трябва да се постави веднага след отстраняване на защитното саше.
За да се предотврати намеса в адхезивните свойства на EVRA, не трябва да се прилагат кремове, лосиони или талк върху областта на кожата, където трябва да се постави трансдермален пластир EVRA.
След употреба трансдермалният пластир все още съдържа значително количество активни съставки. Остатъчните хормонални активни съставки на трансдермалния пластир могат да имат вредни ефекти, ако достигнат водната среда. Следователно използваният трансдермален пластир трябва внимателно да се изхвърли. Етикетът, който да се използва за изтриване. поставен от външната страна на сашето, той трябва да се вдигне. Използваният трансдермален пластир трябва да се постави вътре в отворения етикет за изхвърляне, така че лепкава повърхност да покрива засенчената зона на сашето. След това етикетът трябва да бъде затворен чрез запечатване на използвания трансдермален пластир вътре. Неизползваните лекарства и отпадъците, получени от тези лекарства, трябва да се изхвърлят в съответствие с местните разпоредби. Използваните трансдермални пластири не трябва да се изхвърлят в тоалетната или да се елиминират отпадъците чрез средства за течности.
07.0 Притежател на разрешението за търговия
JANSSEN-CILAG INTERNATIONAL N.V.
Turnhoutseweg, 30
B-2340 Beerse
Белгия
08.0 НОМЕР НА РАЗРЕШЕНИЕТО ЗА ПОТРЕБЕНИЕ
EU/1/02/223/001
035684012
EU/1/02/223/002
035684024
EU/1/02/223/003
035684036
09.0 ДАТА НА ПЪРВО РАЗРЕШЕНИЕ ИЛИ ПОДНОВЯВАНЕ НА РАЗРЕШЕНИЕТО
Дата на първо разрешаване: 22 август 2002 г.
Дата на последното подновяване: 22 август 2012 г.
10.0 ДАТА НА ПРЕГЛЕД НА ТЕКСТА
01/2014