Общност
Лечението на хронична миелоидна левкемия (ХМЛ) включва няколко терапевтични възможности, които могат да държат болестта под контрол за продължителни периоди от време. Рутинните изследвания на кръвта и костния мозък и честата оценка от хематолог или онколог могат да наблюдават прогресията на рака.

От резултатите от медицинските изследвания (кръвна картина, цитогенетични и молекулярни тестове) е възможно да се разбере:
- Степента на ефективност на лечението във времето и развитието на отговора към терапията;
- Ако болестта вече не реагира на лекарства (резистентност към терапия).
Мониторинг и отговор на терапията
Правилното проследяване на хода на заболяването е от съществено значение за проверка на ефикасността на терапията и следователно, за да може да се намеси своевременно в случай на неуспех на лечението.
Цитогенетичният анализ и изследванията на молекулярната биология се използват, както и за диагностични цели, също за оценка на степента на отговор към терапевтичния протокол и за подчертаване на всяка персистираща болест след лечение (изследване на минимално остатъчно заболяване):
- Пълен хематологичен отговор: Когато терапията започне да дава ефект, броят на левкемичните клетки се намалява. Хематологичните тестове вече не могат да откриват аберантни клонинги, но това е възможно с цитогенетичен анализ.
- Пълен цитогенетичен отговор: получен, когато присъствието на филаделфийската хромозома (Ph) вече не се подчертава чрез конвенционален цитогенетичен анализ (стандартен подход за наблюдение на отговора към лечението) или чрез флуоресцентна in situ хибридизация (FISH), техника, която оценява процента на Ph + клетки от костен мозък. Цитогенетичният анализ, извършен върху тънкоиглена аспирирана проба от костен мозък, също е единственият метод за определяне на наличието на каквито и да е хромозомни изменения, в допълнение към филаделфийската хромозома, с прогностична роля.
- Пълен молекулен отговор: достига се, когато молекулярният анализ не е в състояние да открие експресията на хибридния ген BCR / ABL. Терапията се е доказала като ефективна и молекулярните сигнали, които насърчават производството на bcr-abl протеини, са толкова ниски, че не могат да бъдат открити дори при силно чувствителни тестове като молекулярни. Повишените нива на транскрипт, които се наблюдават, могат да показват загуба на отговор на лечението.
Постигането на тези резултати представлява много важен резултат: много проучвания показват, че пациентите с пълен цитогенетичен и молекулен отговор имат много голяма вероятност да оцелеят дълго време, без прогресиране на заболяването до ускорената и / или бластната фаза .
Много фактори могат да повлияят на ефикасността на терапията и поради тази причина в началните етапи се препоръчва да се пристъпи към тестове след 3, 6, 12 и 18 месеца.
Информацията, получена досега от клинични проучвания, които определят оптималния отговор и неуспех по различно време на терапията, са довели до формулирането на схема за мониторинг, която трябва да се следва за правилното управление на пациента (показания, предложени от Европейска мрежа за левкемия):
Хематологът (или онкологът) ще може да установи някои цели и да провери ефикасността на терапията в конкретния клиничен случай, тъй като пациентите реагират различно на терапията и не всички са в състояние да достигнат оптималните терапевтични етапи в предвидения период от време ...
Терапевтични възможности
Основната цел на лечението на ХМЛ е „постигане на пълна молекулярна ремисия: болестта се контролира от лечението (дори и да не изчезне напълно) и броят на произведените патологични клонинги е достатъчно ограничен, за да не предизвика никакви симптоми. Повечето хора не могат премахнете напълно левкемичните клетки, лечението може да помогне за постигане на дългосрочна ремисия на заболяването.
Терапевтичните цели могат да включват:
- Ограничете проявата на симптоми на хронична миелоидна левкемия;
- Възстановяване на нормални параметри, свързани с броя на кръвните клетки;
- Намалете броя на филаделфийските хромозомно -положителни левкемични клетки (Ph +) и молекулярни сигнали (BCR / ABL транскрипти);
- Стремете се към изчезването на филаделфийските + хромозоми (пълен цитогенетичен отговор).
Конвенционални антибластични лекарства
Някои антибластични лекарства, като напр бусулфан (алкилиране) и l "хидроксиурея (специфичен инхибитор на синтеза на ДНК), са били използвани, особено в миналото, за постигане на циторедукция и контрол на заболяването в хроничната фаза. Конвенционалното лечение доведе до подобряване на качеството на живот, но не успя да промени значително естествената история на заболяването или да предотврати прогресирането до ускорена / бластна фаза.
Рекомбинантен интерферон-алфа
От началото на 80 -те години въвеждането на интерферони позволява да се наблюдава, в допълнение към намаляването и нормализирането на гранулоцитния дял, постигането на негативизация на цитогенетичните и молекулярни тестове, предизвиквайки по -голяма продължителност на хроничната фаза, с последващо намаляване на еволюцията в ускорена и / или бластна фаза. Интерферон -алфа е намалил ролята на конвенционалната CML терапия: това лекарство е в състояние да индуцира пълен цитогенетичен отговор при 20-30% от пациентите, като по този начин пречи на транслацията на пролиферативни сигнали в Ph + клетки и инхибира клетъчното размножаване на туморни предшественици. Интерферон-алфа също действа с непряк механизъм върху оцеляването на левкемичните клетки, като намалява тяхната клетъчна адхезия и усилва активността на клетките на имунната система.
Ограничение за употребата на това лекарство е дадено от неговата пренебрежимо токсична токсичност.Страничните ефекти на интерферона включват умора, треска и загуба на тегло. За да се подобрят постигнатите резултати, интерферонът е комбиниран с други цитотоксични агенти. Доказано е, че само връзката на интерферон с цитозин арабинозид (ARA-C) предлага по-добри резултати от интерферон самостоятелно, без обаче очевидно предимство за оцеляване.
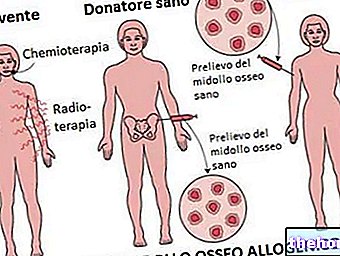
Алогенна трансплантация на костен мозък
Трансплантацията на стволови клетки от здрав донор, съвместима с реципиента (алогенна трансплантация), представлява от години най -честата терапевтична индикация и все още представлява единственото лечение, способно окончателно да изкорени неоплазмата.
Тази процедура, когато се извършва в хронична фаза, може да доведе до петгодишна преживяемост без заболяване в приблизително 50% от случаите.
Алогенната трансплантация на костен мозък включва първа фаза на унищожаване на всички (или почти всички) Ph + клетки чрез кондиционираща терапия (химиотерапия в комбинация с облъчване на цялото тяло), последвана от възстановяване на хемопоетичния мозък от инфузираните донорни стволови клетки. В допълнение, лимфоцитите на донорския мозък допринасят за контролиране и / или елиминиране на всички Ph + клетки с имунно-медииран ефект, наречен „присаден срещу левкемия“ (присаден срещу левкемия) ефект. Отговорът на терапията може да бъде проследен чрез оценка дали молекулярните промени, характерни за хроничната миелоидна левкемия, са изчезнали. Алогенната трансплантация на костен мозък представлява терапевтичното лечение, способно да "излекува" CML, но за съжаление включва степен на неуспех поради фатална токсичност и / или рецидив. Тази процедура всъщност е много взискателна и може да бъде повлияна от възрастта на пациент, пациент и скоростта на трансплантацията (месеци или години от диагнозата на хроничната фаза): поради потенциалната си опасност, тя е практична само при пациенти на възраст под 55 години, без допълнителни съпътстващи патологии. Следователно, алогенната трансплантация представлява реална терапевтична възможност само за малцинство от пациенти с ХМЛ (също като се имат предвид трудностите при намирането на съвместим донор на стволови клетки).
Съвсем наскоро при пациенти с хронична миелоидна левкемия, които не отговарят на условията за алотрансплантация (възраст, липса на донор, отказ и т.н.), беше предложена автотрансплантация. Костният мозък на пациента, реинфузиран след "умишлено адекватна цитоцидна терапия за Ph + клетки (с антибластичен + интерферон), би се възстановил с преобладаващо повторно разширяване на Ph-клетките.
Иматиниб мезилат (Glivec ®)
Историята на лечението на хронична миелоидна левкемия е революционизирана с въвеждането на първия инхибитор на тирозин киназата (иматиниб мезилат), който допринесе значително за подобряване на качеството на живот на пациентите.
Иматиниб е специфичен инхибитор на BCR / ABL, създаден след разбиране на молекулярната биология на заболяването и използван при лечението на Ph + хронична миелоидна левкемия.
Лекарството е в състояние да индуцира пълна молекулярна цитогенетична ремисия при 80-90% от пациентите и също така е активно при миелоидни неоплазми с еозинофилия и участие на PDGRF (тромбоцитен растежен фактор, серумен митоген, участващ в много патологични състояния, което насърчава хемотаксиса и пролиферацията капацитет).
Иматиниб селективно блокира активността на тирозин киназата на BCR / ABL чрез инхибиторен механизъм на АТФ: лекарството свързва високоенергийната молекула (АТФ), налична в специфичния домен на BCR / ABL киназата, предотвратявайки фосфорилирането на други субстрати и блокирайки каскадата реакции, които биха били отговорни за процеса на генериране на Ph + левкемични клонове. Използваната доза на тази молекула (иматиниб метисилат) варира от 400 mg / ден до 800 mg / ден по отношение на фазата на заболяването и отговора. Понастоящем това е лекарството на избор за лечение на ХМЛ поради забележителната си ефикасност. Страничните ефекти, обратими със суспензията и / или намаляването на дозата, могат да бъдат различни (повишени трансаминази, гадене, кожни обриви, задържане на течности и др.).
С течение на времето са наблюдавани случаи, показващи резистентност към лекарството (например пациенти с напреднало заболяване) и са идентифицирани биологично-клинични критерии за определяне на типа отговор на лечението. Механизмите, отговорни за тази резистентност, изглеждат множество (мутации на киназния домен, амплификация / свръхекспресия на BCR / ABL, клонална еволюция ...). В тези случаи продължаването на лечението с иматиниб вече не е подходящо.
За пациенти с тези състояния възможните възможности са:
- Алогенна трансплантация;
- Конвенционална терапия (хидроксиурея, бусулфан и др.);
- L "интерферон;
- Експериментална терапия (с инхибитори на тирозин киназа от второ поколение).
Инхибитори на тирозин киназа от второ поколение
Неуспехът в лечението с иматиниб е свързан с прогресиране на ускорена и / или бластна фаза на хронична миелоидна левкемия и носи особено лоша прогноза. През последните години фармакологичните изследвания позволяват използването в клиничната практика на инхибитори на тирозин киназа от второ поколение, активни при пациенти, които са развили резистентност към иматиниб: Dasatinib (Sprycel ®) и Nilotinib (Tasigna ®) се използват при пациенти с хронична фаза и / или прогресираща CML, рефрактерна на Glivec ® и са в състояние да индуцират отново пълни и устойчиви хематологични, цитогенетични и молекулярни реакции. BCR / ABL киназния домен и се оказват резистентни към различни инхибиторни лекарства. Други молекули в експерименталната фаза (инхибитори от трето поколение) са насочени към специфични мишени на хронична миелоидна левкемия; по -специално, те са способни да сенсибилизират левкемични клетки Ph + със специфични мутации (пример: Mk-0457 за резистентна CML и с мутация на T315I, която пряко засяга мястото на свързване на иматиниб).
Други статии на тема „Терапия с хронична миелоидна левкемия“
- Хронична миелоидна левкемия: Хронична миелоидна левкемия: Диагноза
- Хронична миелоидна левкемия: определение, причини, симптоми





















.jpg)

