Определение
Ензимите са протеини, произведени в растителни и животински клетки, които действат като катализатори, ускоряващи биологичните реакции, без да бъдат модифицирани.
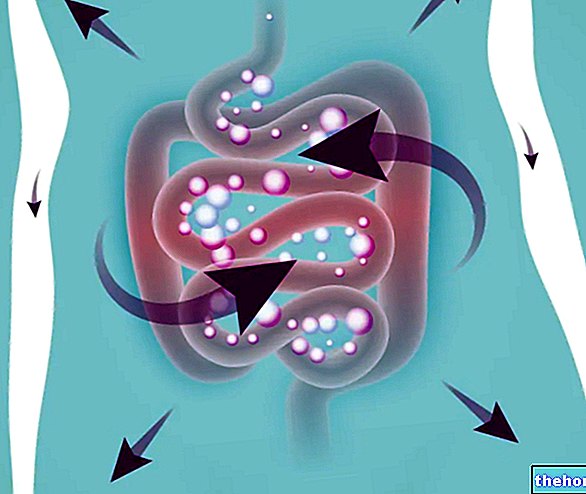
Ензимите действат чрез комбиниране с определено вещество, за да го трансформират в различно вещество; класически примери са дадени от храносмилателни ензими, присъстващи в слюнката, стомаха, панкреаса и тънките черва, които изпълняват съществена функция в храносмилането и помагат за разграждането на храната до основни съставки, които след това могат да бъдат усвоени и използвани от организма, обработени от други ензими или се отделят като отпадъци.
Всеки ензим има специфична роля: този, който разгражда мазнините, например, не действа върху протеини или въглехидрати. Ензимите са от съществено значение за благосъстоянието на организма. Дефицитът, дори на отделен ензим, може да причини сериозни смущения. Добре известен пример е фенилкетонурия (PKU), заболяване, характеризиращо се с невъзможност да се метаболизира незаменима аминокиселина, фенилаланин, натрупването на който може да причини физически деформации и психични заболявания.
Биохимично изследване
Ензимите са специфични протеини, които имат характеристиката, че са биологични катализатори, тоест имат способността да разграждат енергията на активиране (Eatt) на реакцията, променяйки нейния път, така че кинетично бавният процес да е по -бърз.
Ензимите увеличават кинетиката на термодинамично възможните реакции и за разлика от катализаторите те са повече или по -малко специфични: следователно те притежават субстратна специфичност.
Ензимът не участва в стехиометрията на реакцията: за да се случи това, крайното каталитично място трябва да бъде идентично с изходното.
В каталитичното действие почти винаги има бавна фаза, която определя скоростта на процеса.
Когато говорим за ензими, не е правилно да говорим за равновесни реакции, вместо това говорим за стабилно състояние (състояние, при което определен метаболит се образува и консумира непрекъснато, като поддържа концентрацията му почти постоянна във времето). Продуктът от реакция, катализирана от един ензим, обикновено сам по себе си е реагент за последваща реакция, катализиран от друг ензим и т.н.
Процесите, катализирани от ензими, обикновено се състоят от последователности от реакции.
Обща реакция, катализирана от ензим (Е), може да бъде обобщена, както следва:

Е е ензимът
S е субстратът;
ES представлява адукта между ензима и субстрата;
P е продуктът;
K е константата на скоростта на реакцията.
Общ ензим (E) се комбинира със субстрата (S), за да образува адукта (ES) с константа на скоростта K1; той може да се дисоциира обратно в E + S, с константа на скоростта K2, или, (ако "живее" достатъчно дълго ) може да премине към форма P с константа на скоростта K3.
Продуктът (Р) може от своя страна да се рекомбинира с ензима и да реформира адукта с константа на скоростта К4.
Когато ензимът и субстратът се смесят, има част от времето, през което срещата между двата вида все още не е настъпила: тоест има изключително кратък интервал от време (който зависи от реакцията), в който ензимът и субстратът имат все още не е изпълнено; след този период ензимът и субстратът влизат в контакт в нарастващи количества и се образува ES адукт. Впоследствие ензимът действа върху субстрата и продуктът се освобождава. След това може да се каже, че c "е начален интервал от време, в който концентрацията на ES адукта не може да бъде определена; след този период се приема, че стабилно състояние е установено, че скоростта на процесите, които водят до получаване на адукта, е равна на скоростта на процесите, които водят до разрушаване на адукта.
Константата на Михаелис-Ментен (KM) е равновесна константа (посочена към първото равновесие, описано по-горе); може да се каже, с добро приближение (тъй като трябва да се има предвид и K3), че КМ е представено от съотношението между кинетичните константи К2 и К1 (отнасящо се до разрушаването и образуването на адукта ES в първото равновесие, описано по -горе) .
Чрез константата на Michaelis-Menten имаме „индикация за афинитета между ензима и субстрата: ако КМ е малък с“ е „висок афинитет между ензима и субстрата, тогава адуктът на ES е стабилен.
Ензимите подлежат на регулиране (или модулация).
В миналото се говореше главно за отрицателна модулация, тоест инхибиране на каталитичните способности на ензим, но може да има и положителна модулация, тоест има видове, способни да подобрят каталитичните способности на ензим.
Има 4 вида инхибиции (получени от приближения, направени на модел, за да съответстват на експерименталните данни с математически уравнения):
- конкурентно инхибиране
- неконкурентно инхибиране
- неконкурентно инхибиране
- конкурентно инхибиране
Говорим за конкурентно инхибиране, когато молекула (инхибитор) е в състояние да се конкурира със субстрата. За структурно сходство, инхибиторът може да реагира на мястото на субстрата; оттук и терминологията "конкурентно инхибиране". Вероятността ензимът да се свърже с инхибитора или субстрата зависи от концентрацията на двата и техния афинитет с ензима; следователно скоростта на реакцията зависи от тези фактори.
За да се получи същата скорост на реакция като без присъствието на инхибитора, е необходимо да има по -висока концентрация на субстрат.
Експериментално е показано, че в присъствието на инхибитор константата на Михаелис-Ментен се увеличава.
Що се отнася, вместо това, "неконкурентното инхибиране, взаимодействието между молекулата, която трябва да функционира като модулатор (положителен или отрицателен инхибитор) и" ензима, се осъществява на място, различно от това, в което взаимодействието възниква между ензим и субстрат; следователно говорим за алостерична модулация (от гръцки алостерос → друг сайт).
Ако инхибиторът се свърже с ензима, той може да предизвика промяна в структурата на ензима и следователно може да намали ефективността, с която субстратът се свързва с ензима.
При този тип процес константата на Михаелис-Ментен остава постоянна, тъй като тази стойност зависи от равновесието между ензима и субстрата и дори в присъствието на инхибитор, тези равновесия не се променят.
Явлението некомпетентно инхибиране е рядко; типичен неконкурентоспособен инхибитор е вещество, което обратимо се свързва с ES адукта, причинявайки ESI:

Инхибирането от излишък на субстрат понякога може да бъде неконкурентоспособно, тъй като това се случва, когато втора субстратна молекула се свързва с ES комплекса, което води до появата на ESS комплекса.
Компетентният инхибитор, от друга страна, може да се свърже само със субстратния ензимен адукт, както в предишния случай: свързването на субстрата със свободния ензим предизвиква конформационна модификация, която прави мястото достъпно за инхибитора.
Константата на Michaelis Menten намалява с увеличаване на концентрацията на инхибитора: следователно афинитетът на ензима към субстрата се увеличава.
Серинова протеаза
Те са семейство ензими, към които принадлежат химотрипсин и трипсин.
Химотрипсинът е протеолитичен и хидролитичен ензим, който реже вдясно от хидрофобни и ароматни аминокиселини.
Продуктът на гена, който кодира химотрипсин, не е активен (активира се с команда); неактивната форма на химотрипсин е представена от полипептидна верига от 245 аминокиселини. Химотрипсинът има глобуларна форма поради пет дисулфидни моста и други незначителни взаимодействия (електростатични, сили на Ван дер Ваалс, водородни връзки и др.).
Химотрипсинът се произвежда от химозните клетки на панкреаса, където се съдържа в специални мембрани и се изхвърля през панкреатичния канал в червата, по време на смилането на храната: химотрипсинът всъщност е храносмилателен ензим. Протеините и хранителните вещества, които приемаме с храната, се подлагат на храносмилане, за да бъдат редуцирани до по -малки вериги и да бъдат усвоени и трансформирани в енергия (например амилазите и протеазите разграждат хранителните вещества до глюкоза и аминокиселини, които достигат до клетките, през кръвоносните съдове те достигат до порталната вена и оттам се транспортират до черния дроб, където се подлагат на по -нататъшно лечение).
Ензимите се произвеждат в неактивна форма и се активират само когато достигнат „мястото, където трябва да работят“; след като действието им приключи, те се деактивират. Веднъж дезактивиран ензим не може да се активира отново: за да има "допълнително каталитично действие, той трябва да бъде заменен с" друга ензимна молекула. Ако химитрипсинът се произвежда в активна форма вече в панкреаса, той би атакувал последния: панкреатитът е патология, дължаща се на храносмилателни ензими, които вече са активирани в панкреаса (а не в необходимите места); някои от тях, ако не се лекуват навреме, водят до смърт.
В химотрипсина и във всички серинови протеази каталитичното действие се дължи на наличието на алкохолен анион (-СН2О-) в страничната верига на серин.
Сериновите протеази приемат това име именно защото тяхното каталитично действие се дължи на серин.
След като всички ензими са изпълнили действието си, преди да могат отново да оперират върху субстрата, той трябва да бъде възстановен с вода; "освобождаването" на серин от водата е най-бавният етап от процеса и именно тази фаза което определя скоростта на катализа.
Каталитичното действие протича в две фази:
- образуване на аниона с каталитични свойства (анион алкохолат) и последваща нуклеофилна атака върху карбонилния въглерод (С = О) с разцепване на пептидната връзка и образуване на естера;
- водна атака с възстановяване на катализатора (в състояние отново да прояви каталитичното си действие).
Различните ензими, принадлежащи към семейството на сериновите протеази, могат да бъдат съставени от различни аминокиселини, но за всички тях каталитичното място е представено от алкохолен анион от страничната верига на серин.
Подсемейство серинови протеази е това на ензимите, участващи в коагулацията (което се състои в трансформацията на протеина, от тяхната неактивна форма в "друга активна форма). Тези ензими гарантират, че коагулацията е възможно най -ефективна и е ограничена в пространството и времето (коагулацията трябва да се случи бързо и трябва да се случи само в близост до увредената зона). Ензимите, участващи в коагулацията, се активират в каскада (от активирането на един ензим се получават милиарди ензими: всеки активиран ензим , от своя страна активира много други ензими).
Тромбозата е патология, дължаща се на неправилно функциониране на коагулационните ензими: причинява се от активирането, без необходимост (тъй като няма нараняване), на ензимите, използвани при коагулацията.
Съществуват модулиращи (регулаторни) ензими и инхибиращи ензими за други ензими: взаимодействайки с последните, те регулират или инхибират тяхната активност; дори продуктът на ензим може да бъде инхибитор на ензима.Има и ензими, които действат колкото повече, толкова по -голям е субстратът.
Лизозим
Луиджи Пастьор открил, чрез кихане върху чиния на Петри, че в слузта има ензим, способен да убива бактериите: лизозим; от гръцки: liso = какъв размер; zimo = ензим.
Лизозимът е способен да разруши клетъчната стена на бактериите. Бактериите и едноклетъчните организми като цяло се нуждаят от механично устойчиви структури, които ограничават формата им; вътре в бактериите има много високо осмотично налягане, така че те привличат вода. Плазмената мембрана би се взривила, ако няма клетъчна стена, която да се противопоставя на навлизането на вода и да ограничава обема на бактерията.
Клетъчната стена се състои от полизахаридна верига, в която се редуват молекули на N-ацетил-глюкозамин (NAG) и молекули на N-ацетил-мурамична киселина (NAM); връзката между NAG и NAM се разрушава чрез хидролиза.Карбоксилната група на NAM, в клетъчната стена, участва в пептидна връзка с аминокиселина.
Между различните вериги се образуват мостове, състоящи се от псевдопептидни връзки: разклонението се дължи на молекулата на лизина; структурата като цяло е много разклонена и това й придава висока стабилност.
Лизозимът е антибиотик (убива бактериите): действа, като прави пукнатина в бактериалната стена; когато тази структура (която е механично устойчива) се счупи, бактерията изтегля вода, докато не се спука. Лизозимът успява да разруши β-1,4 глюкозидната връзка между NAM и NAG.
Каталитичното място на лизозима е представено от жлеб, който минава по протежение на ензима, в който е вмъкната полизахаридната верига: шест глюкозидни пръстена на веригата са поставени в жлеба.
В позиция три на канала c "е дросел: в това положение може да се постави само един NAG, тъй като NAM, който е с по -големи размери, не може да влезе. Действителното каталитично място е между позиции четвърта и пета: тъй като има a NAG в позиция три, изрязването ще се извърши между NAM и NAG (а не обратно); следователно изрязването е специфично.
Оптималното рН за действие на лизозима е пет. В каталитичното място на ензима, т.е. между позиции четвърто и пето, има страничните вериги на аспарагинова киселина и глутаминова киселина.
Степен на хомология: измерва родството (т.е. сходството) между протеиновите структури.
Съществува силна връзка между лизозим и лактоза-синтаза.
Лактоза синтетазата синтезира лактоза (която е основната млечна захар): лактозата е галактозил глюкозид, в който c "е β-1,4 глюкозидна връзка между галактозата и глюкозата.
Следователно, лактоза синтетазата катализира реакцията, обратна на тази, катализирана от лизозим (който вместо това разцепва β-1,4 глюкозидната връзка)
Лактоза синтетазата е димер, тоест изградена е от две протеинови вериги, едната от които има каталитични свойства и е сравнима с лизозима, а другата е регулаторна субединица.
По време на бременност гликопротеините се синтезират от клетките на млечната жлеза под действието на галатозил-трансфераза (има "хомология на последователността от 40% с лизозим): този ензим е в състояние да прехвърли галактозилна група от високоенергийна структура към структура на гликопротеин.По време на бременността се индуцира експресията на гена, който кодира галактозил-трансфераза (има и експресия на други гени, които също дават други продукти): има увеличаване на размера на гърдата, защото се активира млечната жлеза (по-рано неактивна), която трябва да произвежда мляко. По време на раждането се произвежда α-лакталбумин, който е регулаторен протеин: той е в състояние да регулира каталитичния капацитет на галактозил-трансферазата (чрез дискриминация на субстрата). Галактозил-трансферазата, модифицирана от α-лакталалбумин, е в състояние да прехвърли галактозил върху глюкозна молекула: образувайки β-1,4 гликозидна връзка и давайки лактоза (лактоза синтетаза).
Следователно, галактозната трансфераза подготвя млечната жлеза преди раждането и произвежда мляко след раждането.
За да произвежда гликопротеини, галактозил трансферазата се свързва с галактозил и NAG; по време на раждането лакталният албумин се свързва с галактозилтрансферазата, като последният разпознава глюкозата и вече не NAG да дава лактоза.













.jpg)