Активни съставки: естрадиол (естрадиол валерат), диеногест
KLAIRA филмирани таблетки
Защо се използва Qlaira? За какво е?
- Qlaira е противозачатъчно хапче и се използва за предотвратяване на бременност.
- Qlaira се използва за лечение на тежки периоди (не причинени от заболяване на матката) при жени, които желаят да използват орална контрацепция.
- Всяка цветна активна таблетка съдържа малко количество женски хормони, естрадиол валерат или естрадиол валерат, комбинирани с диеногест.
- Двете бели таблетки не съдържат никакви активни съставки и се наричат неактивни таблетки.
- Хапчетата за контрацепция, които съдържат два хормона, се наричат още „комбинирани хапчета“.
Противопоказания Когато Qlaira не трябва да се използва
Когато не трябва да приемате Qlaira Не използвайте Qlaira, ако имате някое от изброените по -долу състояния. Ако имате някое от изброените по -долу състояния, моля, свържете се с Вашия лекар. Вашият лекар ще обсъди с Вас други методи за контрол на раждаемостта, които може да са по -подходящи за Вас.
Не приемайте Qlaira:
- ако имате (или някога сте имали) кръвен съсирек в кръвоносен съд на крака (дълбока венозна тромбоза, ДВТ), белия дроб (белодробна емболия, РЕ) или други органи;
- ако знаете, че имате нарушение, което засяга съсирването на кръвта, като например дефицит на протеин С, дефицит на протеин S, дефицит на антитромбин-III, фактор V Leiden или антифосфолипидни антитела;
- ако ви предстои операция или ако ще лежите дълго време (вижте раздел „Кръвни съсиреци“);
- ако някога сте имали инфаркт или инсулт;
- ако имате (или някога сте имали) стенокардия (състояние, което причинява силна гръдна болка и може да бъде първи признак на инфаркт) или преходна исхемична атака (TIA - временни симптоми на инсулт);
- ако имате някое от следните заболявания, които биха могли да увеличат риска от образуване на кръвни съсиреци в артериите: - тежък диабет с увреждане на кръвоносните съдове - много високо кръвно налягане - много високо ниво на мазнини (холестерол или триглицериди) в кръвта - заболяване, известно като хиперхомоцистеинемия
- ако имате (или някога сте имали) вид мигрена, наречена "мигрена с аура";
- ако имате (или някога сте имали) „възпаление на панкреаса (панкреатит)
- ако имате (или някога сте имали) чернодробно заболяване и чернодробната Ви функция все още е ненормална
- ако имате (или някога сте имали) рак на черния дроб
- ако имате (или някога сте имали) рак или ако подозирате, че имате рак на гърдата или органите
- ако имате необяснимо вагинално кървене
- ако сте алергични (свръхчувствителни) към естрадиол валерат или диеногест или към някоя от останалите съставки на това лекарство (изброени в точка 6.) Това може да причини сърбеж, обрив или подуване.
Предпазни мерки при употреба Какво трябва да знаете, преди да приемете Qlaira
Общи бележки
Преди да започнете да използвате Qlaira, трябва да прочетете информацията за кръвни съсиреци в раздел 2. Особено важно е да прочетете симптомите на кръвен съсирек (вижте точка 2 "Кръвни съсиреци").
Преди да приемете Qlaira, Вашият лекар ще Ви зададе няколко въпроса относно Вашата лична медицинска история и тази на членовете на Вашето семейство. Лекарят ще измери и кръвното Ви налягане и в зависимост от Вашето лично положение може да извърши и други изследвания.
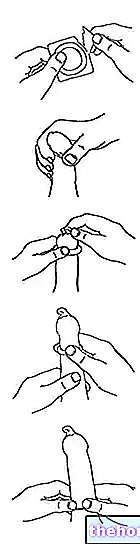
Тази листовка описва различни ситуации, при които употребата на Qlaira трябва да бъде прекратена или когато надеждността на Qlaira може да бъде намалена. В такива ситуации е необходимо да се въздържате от полов акт или да предприемете допълнителни нехормонални контрацептивни мерки, като презервативи или други бариерни методи. Не използвайте метода на ритъма или метода на базалната температура. Всъщност тези методи може да са недостатъчни, тъй като Клайра променя месечните промени в телесната температура и цервикалната слуз.
Както всички хормонални контрацептиви, Клайра не предлага защита срещу HIV инфекция (СПИН) или други болести, предавани по полов път.
Предупреждения и предпазни мерки
Кога трябва да посетите лекар?
Спешно се свържете с лекар
- ако забележите възможни признаци на кръвен съсирек, които могат да показват, че страдате от кръвен съсирек в крака (дълбока венозна тромбоза), кръвен съсирек в белия дроб (белодробна емболия), инфаркт или инсулт (вижте раздел по -долу "Кръвен съсирек").
За описание на симптомите на тези сериозни странични ефекти отидете в раздела „Как да разпознаем кръвен съсирек“.
Уведомете Вашия лекар, ако някое от следните се отнася за Вас.
В някои ситуации трябва да бъдете особено внимателни, когато използвате Qlaira или друг комбиниран орален контрацептив и може да се наложи Вашият лекар да Ви посещава редовно. Ако това състояние се появи или се влоши, докато използвате Qlaira, трябва да кажете на Вашия лекар:
- ако близък роднина има или е имал рак на гърдата
- ако имате заболяване на черния дроб или жлъчния мехур
- ако имате жълтеница
- ако имате диабет
- ако страдате от депресия
- ако имате болест на Crohn или улцерозен колит (хронично възпалително заболяване на червата);
- ако имате системен лупус еритематозус (SLE, заболяване, което засяга естествената защитна система);
- ако имате хемолитично -уремичен синдром (HUS, нарушение на кръвосъсирването, причиняващо бъбречна недостатъчност);
- ако имате сърповидно -клетъчна анемия (наследствено заболяване на червените кръвни клетки);
- ако имате високи нива на мазнини в кръвта (хипертриглицеридемия) или „фамилна анамнеза за това състояние.“ Хипертриглицеридемията е свързана с повишен риск от развитие на панкреатит (възпаление на панкреаса);
- ако ще Ви предстои "операция или ако ще лежите дълго време (вижте раздел 2" Кръвни съсиреци ");
- ако току -що сте родили, рискът от образуване на кръвни съсиреци е по -висок. Попитайте Вашия лекар колко време след раждането можете да започнете да приемате Qlaira;
- ако имате „възпаление на вените под кожата (повърхностен тромбофлебит);
- ако имате разширени вени.
- ако имате епилепсия (вижте раздел "Други лекарства и Qlaira")
- ако имате заболяване, което се е появило за първи път по време на бременност или по време на предишна употреба на полови хормони, например загуба на слуха, порфирия (нарушение на кръвта), херпес гестация (обрив с мехури по време на бременност), хорея на Sydenham (нервно заболяване, при което внезапно тялото възникват движения)
- ако имате (или някога сте имали) петна с жълто-кафява пигментация, известна като „маска за бременност“, особено по лицето (хлоазма). В този случай избягвайте директното излагане на слънчева светлина или ултравиолетови лъчи
- ако страдате от наследствен ангиоедем. Ако забележите симптоми на ангиоедем като подуване на лицето, езика и / или фаринкса и / или затруднено преглъщане или копривна треска със затруднено дишане, незабавно се консултирайте с Вашия лекар.Лекарствата, съдържащи естроген, могат да предизвикат или влошат симптомите на ангиоедем.
- ако имате сърдечна или бъбречна недостатъчност.
Консултирайте се с Вашия лекар, преди да приемете Qlaira.
КРЪВНИ СЪСИРЕЦИ
Използването на комбиниран хормонален контрацептив като Qlaira увеличава риска от образуване на кръвен съсирек в сравнение с неизползването му. В редки случаи кръвен съсирек може да блокира кръвоносните съдове и да причини сериозни проблеми.
Могат да се развият кръвни съсиреци
- във вените (наречени "венозна тромбоза", "венозна тромбоемболия" или ВТЕ)
- в артериите (наричани „артериална тромбоза“, „артериална тромбоемболия“ или АТЕ).
Възстановяването от кръвни съсиреци не винаги е пълно. Рядко могат да се появят дълготрайни тежки ефекти или много рядко те могат да бъдат фатални.
Важно е да запомните, че общият риск от вреден кръвен съсирек, свързан с Qlaira, е нисък.
КАК ДА РАЗПОЗНАЕТЕ КРЪВЕН КРЪВ
Незабавно посетете лекар, ако забележите някой от следните признаци или симптоми.
- подуване на единия крак или по вената на крака или стъпалото, особено когато е придружено от:
- болка или болезненост в крака, които могат да се усетят само когато стоите или ходите
- повишено усещане за топлина в засегнатия крак
- промяна в цвета на кожата на крака, като например бледо, червено или синьо
- задух или внезапно, необяснимо бързо дишане;
- внезапна кашлица без очевидна причина, евентуално причиняваща отделяне на кръв;
- остра болка в гърдите, която може да се увеличи с дълбоко дишане;
- силно замайване или замаяност;
- ускорен или неравномерен сърдечен ритъм;
- силна болка в стомаха
- незабавна загуба на зрение или
- безболезнено замъгляване на зрението, което може да прогресира до загуба на зрение
- болка в гърдите, дискомфорт, чувство на натиск или тежест
- усещане за притискане или пълнота в гърдите, ръката или под гръдната кост;
- чувство на ситост, лошо храносмилане или задушаване;
- дискомфорт в горната част на тялото, излъчващ към гърба, челюстта, гърлото, ръцете и стомаха;
- изпотяване, гадене, повръщане или замаяност;
- крайна слабост, тревожност или задух;
- бърз или неравномерен сърдечен ритъм
- внезапно изтръпване или слабост на лицето, ръката или крака, особено от едната страна на тялото;
- внезапно объркване, трудности при говорене или разбиране;
- внезапно затруднено виждане в едното или в двете очи;
- внезапно затруднено ходене, замаяност, загуба на равновесие или координация;
- внезапна, тежка или продължителна мигрена без известна причина;
- загуба на съзнание или припадък със или без припадъци.
- подуване и бледосиньо обезцветяване на един "крайник";
- силна стомашна болка (остър корем)
КРЪВНИ КРЪВИ ВЪВ ВЕНА
Какво може да се случи, ако във вената се образува кръвен съсирек?
- Използването на комбинирани хормонални контрацептиви е свързано с повишен риск от образуване на кръвни съсиреци във вените (венозна тромбоза). Тези странични ефекти обаче са редки. В повечето случаи те се появяват през първата година от употребата на комбиниран хормонален контрацептив.
- Ако кръвен съсирек се образува във вена на крака или стъпалото, това може да причини дълбока венозна тромбоза (ДВТ).
- Ако кръвен съсирек пътува от крака и се засели в белия дроб, това може да причини "белодробна емболия".
- Много рядко съсирек може да се образува в друг орган като окото (тромбоза на вената на ретината).
Кога е най -висок рискът от образуване на кръвен съсирек във вена?
Рискът от образуване на кръвен съсирек във вена е най -висок през първата година от приемането на комбиниран хормонален контрацептив за първи път. Рискът може да бъде още по -висок, ако рестартирате приема на комбиниран хормонален контрацептив (същото лекарство или различно лекарство) след почивка от 4 или повече седмици.
След първата година рискът се намалява, но винаги е малко по -висок, отколкото ако не сте използвали комбиниран хормонален контрацептив.
Когато спрете приема на Qlaira, рискът от образуване на кръвен съсирек се нормализира в рамките на няколко седмици.
Какъв е рискът от образуване на кръвен съсирек?
Рискът зависи от естествения ви риск от ВТЕ и от вида комбиниран хормонален контрацептив, който приемате.
Общият риск от развитие на кръвен съсирек в крака или белия дроб (DVT или PE) с Qlaira е нисък.
- От 10 000 жени, които не използват никакви комбинирани хормонални контрацептиви и които не са бременни, около 2 ще развият кръвен съсирек за една година.
- От 10 000 жени, които използват комбиниран хормонален контрацептив, който съдържа левоноргестрел, норетистерон или норгестимат, около 5-7 ще развият кръвен съсирек за една година.
- Все още не е известно как рискът от образуване на кръвен съсирек с Qlaira се сравнява с риска, свързан с комбиниран хормонален контрацептив, съдържащ левоноргестрел.
- Рискът от образуване на кръвен съсирек зависи от Вашата медицинска история (вижте „Фактори, които увеличават риска от образуване на кръвен съсирек“).
Фактори, които увеличават риска от образуване на кръвен съсирек във вената
Рискът от образуване на кръвен съсирек с Qlaira е нисък, но някои състояния увеличават риска. Рискът му е по -голям:
- ако имате тежко наднормено тегло (индекс на телесна маса или ИТМ над 30 kg / m2);
- ако близък роднина е имал кръвен съсирек в крака, белия дроб или друг орган в млада възраст (по -малко от около 50 години). В този случай може да имате наследствено разстройство на кръвосъсирването;
- ако Ви предстои операция или ако трябва да лежите дълго време поради нараняване или заболяване или ако имате крак в гипс. Може да се наложи да спрете приема на Qlaira няколко седмици преди операцията или по време на периодът, в който сте по -малко подвижни. Ако трябва да спрете приема на Qlaira, попитайте Вашия лекар кога можете да започнете да го приемате отново;
- с напредване на възрастта (особено след 35 -годишна възраст);
- ако сте родили преди по -малко от няколко седмици.
Рискът от образуване на кръвен съсирек се увеличава, колкото повече състояния имате от този тип.
Пътуването със самолет (продължително> 4 часа) може временно да увеличи риска от образуване на кръвен съсирек, особено ако имате някои от изброените други рискови фактори.
Важно е да кажете на Вашия лекар, ако някое от изброените се отнася за Вас, дори ако не сте сигурни. Вашият лекар може да реши, че Qlaira трябва да бъде спрян.
Ако някое от горните състояния се промени, докато използвате Qlaira, например, ако близък роднина има тромбоза без известна причина или ако наддавате много, свържете се с Вашия лекар.
КРЪВНИ КРЪВИ В АРТЕРИЯ
Какво може да се случи, ако кръвен съсирек се образува в "артерия"?
Подобно на кръвни съсиреци във вена, съсиреците в артерията могат да причинят сериозни проблеми, например могат да причинят инфаркт или инсулт.
Фактори, които увеличават риска от образуване на кръвен съсирек в артерията
Важно е да се отбележи, че рискът от инфаркт или инсулт, свързан с употребата на Qlaira, е много нисък, но може да се увеличи:
- с увеличаване на възрастта (над 35 години);
- ако пушите. Когато използвате комбиниран хормонален контрацептив като Qlaira, се препоръчва да спрете да пушите. Ако не можете да спрете да пушите и сте на възраст над 35 години, Вашият лекар може да Ви посъветва да използвате различен вид контрацептив;
- ако сте с наднормено тегло;
- ако имате високо кръвно налягане;
- ако член на вашето близко семейство е имал инфаркт или инсулт в ранна възраст (по -малко от около 50 години). В този случай може да имате и висок риск от инфаркт или инсулт;
- ако вие или ваш близък роднина имате високо ниво на мазнини в кръвта (холестерол или триглицериди);
- ако страдате от мигрена, особено мигрена с аура;
- ако имате някакви сърдечни проблеми (дефект на клапана, нарушение на сърдечния ритъм, наречено предсърдно мъждене);
- ако имате диабет.
Ако имате повече от едно от тези състояния или ако някое от тях е особено тежко, рискът от образуване на кръвен съсирек може да бъде дори по -висок.
Ако някое от горните състояния се промени, докато използвате Qlaira, например, ако започнете да пушите, ако близък роднина има тромбоза без известна причина или ако наддавате много, свържете се с Вашия лекар.
Клайра и рак
Рак на гърдата се наблюдава малко по -често при жени, използващи комбинирано хапче, но не е известно дали това се дължи на лечението. Например, при жените, използващи комбинираните хапчета, може да се открият повече видове рак, тъй като те се наблюдават по -често. Рискът от рак на гърдата постепенно намалява след спиране на комбинираната хормонална контрацепция Важно е да проверявате редовно гърдите си и трябва да се свържете с Вашия лекар, ако усетите някаква бучка.
Доброкачествени чернодробни тумори са наблюдавани в редки случаи при жени, използващи хапчета, и още по -рядко злокачествени чернодробни тумори. В единични случаи тези тумори са довели до животозастрашаващо вътрешно кървене. Свържете се с Вашия лекар, ако почувствате особено силна коремна болка.
Някои проучвания показват, че продължителната употреба на хапчето увеличава риска от развитие на рак на маточната шийка, но не е ясно до каква степен сексуалното поведение или други фактори като човешки папиломен вирус (HPV) увеличават този риск.
Междуменструално кървене
През първите няколко месеца от приема на Qlaira може да възникне неочаквано кървене. Кървенето обикновено започва на 26 -ия ден, в деня, в който сте взели втората си тъмночервена таблетка, или в следващите дни. Информацията, предоставена от дневниците, водени от жените по време на клинично проучване с Qlaira, показва, че не е необичайно да има неочаквано кървене в даден цикъл (10-18% от потребителите). Ако неочаквано кървене настъпи за повече от 3 последователни месеца, или ако тези се появят след няколко месеца, лекарят трябва да проучи причината.
Какво да направите, ако менструацията не се появи на 26 или следващите дни
Информацията, предоставена от дневниците, водени от жените по време на клинично проучване с Qlaira, показва, че не е необичайно на 26 -ия ден да не настъпи менструация (наблюдава се в приблизително 15% от циклите).
Ако сте приели правилно всички таблетки, не сте имали повръщане или тежка диария и не сте приемали други лекарства, е малко вероятно да сте бременна.
Ако менструацията не се появи два пъти подред или ако не сте приели правилно таблетките, може да сте бременна. Свържете се незабавно с Вашия лекар. Не започвайте следващата опаковка, докато не сте сигурни, че сте изключили бременността.
Взаимодействия Кои лекарства или храни могат да променят ефекта на Qlaira
Винаги информирайте Вашия лекар или фармацевт, ако приемате или наскоро сте приемали други лекарства или билкови лекарства, включително тези, отпускани без рецепта. Също така кажете на всеки друг лекар или зъболекар, който предписва други лекарства (или фармацевта), че приемате Qlaira. Те могат да ви кажат дали трябва да предприемете допълнителни контрацептивни мерки (например презервативи) и ако да, за колко време.
Някои лекарства влияят на кръвните нива на Qlaira и могат да го направят по -малко ефективен при предотвратяване на бременност или да причинят неочаквано кървене. Те включват:
o лекарства, използвани за лечение на:
- епилепсия (напр. примидон, фенитоин, барбитурати, карбамазепин, окскарбазепин, топирамат, фелбамат),
- туберкулоза (напр. рифампицин),
- ХИВ и вирусна инфекция с хепатит С (ритонавир, невирапин, ефавиренц, известни като протеазни инхибитори и ненуклеозидни инхибитори на обратната транскриптаза), други инфекции (гризеофулвин).
или препарати на базата на жълт кантарион (Hypericum Perforatum)
Някои лекарства могат да повишат нивата на активните вещества на Qlaira в кръвта. Уведомете Вашия лекар, ако използвате:
- противогъбични лекарства, съдържащи кетоконазол,
- антибиотици, съдържащи еритромицин.
Qlaira може да повлияе ефекта на други лекарства, например:
- лекарства, съдържащи циклоспорин,
- антиепилептичният ламотрижин (това може да причини увеличаване на честотата на гърчовете).
Посъветвайте се с Вашия лекар или фармацевт, преди да приемете каквото и да е лекарство.Вашият лекар или фармацевт може да Ви каже дали трябва да предприемете допълнителни защитни мерки, докато приемате Qlaira заедно с други лекарства.
Klaira с храна и напитки
Qlaira може да се приема със или без храна, ако е необходимо с малко количество вода.
Лабораторен анализ
Ако се нуждаете от кръвен тест или други лабораторни изследвания, кажете на Вашия лекар или лабораторен персонал, че приемате хапчето, тъй като оралните контрацептиви могат да повлияят на резултатите от някои изследвания.
Предупреждения Важно е да знаете, че:
Бременност и кърмене
По време на бременност не трябва да използвате Qlaira. Ако забременеете, докато приемате Qlaira, трябва незабавно да спрете лечението и да се свържете с Вашия лекар.Ако искате да забременеете, можете да спрете приема на Qlaira по всяко време (вижте също „Ако спрете приема на Qlaira“).
Употребата на Qlaira обикновено не се препоръчва по време на кърмене. Ако искате да вземете хапчето по време на кърмене, ще трябва да се свържете с Вашия лекар.
Посъветвайте се с Вашия лекар или фармацевт, преди да приемете каквото и да е лекарство по време на бременност или кърмене.
Шофиране и работа с машини
Няма причина да се смята, че Qlaira влияе върху способността за шофиране или работа с машини.
Qlaira съдържа лактоза
Ако Вашият лекар Ви е казал, че имате „непоносимост към някои захари, свържете се с него, преди да приемете този лекарствен продукт.
Доза, метод и време на приложение Как да използвате Qlaira: Дозировка
Всяка опаковка съдържа 26 цветни активни таблетки и 2 бели неактивни таблетки.
Приемайте по една таблетка Qlaira всеки ден с малко количество течност, ако е необходимо. Можете да приемате таблетките със или без храна, но трябва да ги приемате приблизително по едно и също време всеки ден.
Подготовка на опаковката
За да ви помогне да спазвате правилната последователност, всяка опаковка от Klaira съдържа 7 самозалепващи се етикета със 7-те дни от седмицата.
Изберете стикера за седмицата, който започва с деня, в който започнете да приемате таблетките си. Например, ако започва в сряда, използвайте стикера, който започва с „СРЕДА“.
Прикрепете седмичния стикер към цялата дължина на горната част на опаковката Qlaira, където пише "Поставете стикер тук", така че първият ден да е върху таблета с маркировка "1".
По този начин над всяка таблетка е посочен ден и можете да проверите дали сте приели хапчето в даден ден.Следвайте посоката на стрелката на опаковката, докато всичките 28 таблетки бъдат взети.
Вашият период, наричан още кървене при отнемане, обикновено започва, когато приемате втората тъмночервена таблетка или белите таблетки и може да не е приключил преди да започне следващата опаковка. Някои жени все още имат менструация дори след като са взели първите таблетки от новата опаковка.
Започвате следващата опаковка без почивка, т.е. деня след като приключите с текущата опаковка, дори ако менструацията ви още не е приключила. Това означава, че трябва да започнете следващата опаковка в същия ден от седмицата и менструацията ви трябва да настъпи на същите дни всеки месец ..
Ако използвате Qlaira по този начин, контрацептивното действие е гарантирано дори през 2 -те дни, през които приемате неактивните таблетки.
Кога можете да започнете първата опаковка
- Ако през предходния месец не сте използвали хормонални контрацептиви, започнете да приемате Qlaira през първия ден от менструацията (първия ден от менструацията).
- Промяна от друго комбинирано орално контрацептивно хапче или вагинален пръстен или пластир, комбиниран контрацептив. Започнете да приемате Qlaira ден след последната активна таблетка (последната таблетка, съдържаща активните съставки) от предишното хапче. започнете да използвате Qlaira в деня на отстраняване или следвайте съветите на Вашия лекар.
- Преминаване от метод само с прогестаген (хапче само с прогестаген, инжекция, имплант или освобождаващ прогестоген IUS) Можете да преминете към Qlaira всеки ден от хапче само с прогестоген (от имплант или IUS в деня на отстраняването му, от инжектирането, когато следващата инжекция ще бъде насрочена), но във всички тези случаи трябва да предприемете допълнителни контрацептивни мерки (например презервативи) през първите 9 дни, когато използвате Qlaira.
- След спонтанен аборт Следвайте съветите на Вашия лекар.
- След раждане. Можете да започнете да приемате Qlaira между 21 -ия и 28 -ия ден след раждането. Ако започнете да приемате Qlaira по -късно от 28 -ия ден, използвайте бариерен метод (например презерватив) през първите няколко дни. 9 дни на приема на Qlaira. Ако след раждане сте имали полов акт преди започване на Qlaira, трябва или да изключите бременността, или да изчакате следващата си менструация. Ако искате да започнете Qlaira след забременяване и кърмене, прочетете раздела „Бременност и кърмене ".
Посъветвайте се с Вашия лекар, ако не сте сигурни кога да започнете.
Предозиране Какво да направите, ако сте приели твърде много Qlaira
Ако сте приели повече от необходимата доза KLAIRA
Няма съобщения за сериозни вредни ефекти, ако приемате няколко таблетки Qlaira.
Ако вземете няколко таблетки наведнъж, може да се почувствате зле или да повръщате. The
Младите момичета могат да получат вагинално кървене.
Ако сте пропуснали да приемете QLAIRA
Неактивни таблетки: ако забравите бяла таблетка (двете таблетки в края на опаковката), не е необходимо да ги приемате по -късно, тъй като те не съдържат никакви активни съставки.Важно е обаче да изхвърлите забравената бяла таблетка, за да сте сигурни, че броят на дните на приемане на неактивните таблетки не се е увеличил; това ще увеличи риска от бременност. Продължете със следващата таблетка в обичайното време.
Активни таблетки: В зависимост от деня на цикъла, в който активната таблетка е забравена, тя трябва да предприеме допълнителни мерки за контрацепция, например бариерен метод като презерватив. Вземете таблетките, като следвате указанията по -долу. За подробности вижте също диаграмата по -долу:
- Ако сте закъснели с приемането на таблетка с по -малко от 12 часа, контрацептивната защита не се намалява. Вземете таблетката веднага щом си спомните и след това вземете следващите таблетки, както е планирано.
- Ако забавянето на приема на таблетка е повече от 12 часа, контрацептивната защита може да бъде намалена. В зависимост от деня на цикъла, в който е настъпила забравата, трябва да се използват допълнителни контрацептивни мерки, като бариерен метод, като например презерватив. Вижте също диаграмата по -долу.
- Забравени повече от една таблетка в опаковка Свържете се с Вашия лекар.
Не трябва да приемате повече от две активни таблетки за един ден.
Ако сте пропуснали да започнете нова опаковка или сте забравили една или повече таблетки в рамките на 3-9 дни от опаковката, съществува риск да сте бременна (ако сте правили секс през 7-те дни преди да забравите таблетка) В този случай, моля, свържете се с Вашия лекар. Колкото по-голям е броят на пропуснатите таблетки (особено тези в дни 3-24) и колкото по-близо е това до фазата на неактивна таблетка, толкова по-голям е рискът от намалена контрацептивна защита. подробности, вижте също диаграмата по -долу.
Ако сте забравили някоя от активните таблетки в опаковка и не сте имали менструация в края на опаковката, може да сте бременна. Говорете с Вашия лекар, преди да започнете следващата опаковка.
Употреба при деца
Няма данни за юноши под 18 години.
Какво да направите в случай на повръщане или тежка диария
Ако повръщате в рамките на 3-4 часа след приемането на активна таблетка или имате тежка диария, възможно е активните съставки на хапчето да не се абсорбират напълно от тялото ви.забравете да вземете таблетка.
След повръщане или тежка диария ще трябва да вземете следващата таблетка възможно най -скоро. Ако е възможно в рамките на 12 часа от обичайното време за приемане на хапчето. Ако това е невъзможно или ако вече са минали 12 часа, трябва да следвате инструкциите в „Ако сте пропуснали да приемете Qlaira“. Вземете съответната таблетка от друг опаковка.
Ако спрете приема на Qlaira
Можете да спрете приема на Qlaira по всяко време. Ако все пак искате да избегнете забременяване, попитайте Вашия лекар за съвет относно други безопасни методи за контрацепция. Ако искате да забременеете, спрете приема на Qlaira и изчакайте период преди да опитате. бременност. Това ще ви позволи по -точно да изчислите очакваната дата на доставка.
Ако имате допълнителни въпроси относно употребата на Qlaira, попитайте Вашия лекар или фармацевт.
Странични ефекти Какви са страничните ефекти на Qlaira
Както всички лекарства, Qlaira може да предизвика нежелани реакции, въпреки че не всеки ги получава. Ако получите някакви нежелани реакции, особено ако са тежки или продължителни, или ако има някаква промяна в здравето Ви, която смятате, че може да се дължи на Qlaira, моля, уведомете Вашия лекар.
Повишен риск от образуване на кръвни съсиреци във вените (венозна тромбоемболия (ВТЕ)) или кръвни съсиреци в артериите (артериална тромбоемболия (АТЕ)) е налице при всички жени, приемащи комбинирани хормонални контрацептиви. За по -подробна информация относно различните рискове от „приемането на комбинирани хормонални контрацептиви, вижте раздел 2„ Какво трябва да знаете, преди да използвате Qlaira ”.
Сериозни странични ефекти
Сериозните реакции, свързани с „употребата на хапчета, както и свързаните с тях симптоми, са описани в следните раздели:„ Кръвни съсиреци “и„ Klaira и рак. “Прочетете внимателно тези раздели и незабавно се консултирайте с Вашия лекар, ако е необходимо.
Други възможни странични ефекти
Следните нежелани реакции са свързани с употребата на Qlaira:
Чести нежелани реакции (между 1 и 10 потребители на 100)
- главоболие
- коремна болка, гадене
- акне
- липса на менструация, дискомфорт в гърдите, болезнена менструация, нередовни менструации (с обилно нередовно кървене)
- качване на тегло.
Нечести нежелани реакции (между 1 и 10 потребители на 1 000)
- гъбична инфекция, гъбична инфекция на вулвата и влагалището, вагинална инфекция
- повишен апетит
- депресия, депресивно настроение, емоционално разстройство, затруднено заспиване, намалено сексуално желание, психично разстройство, промени в настроението
- замаяност, мигрена
- горещи вълни, високо кръвно налягане
- диария, повръщане
- повишени чернодробни ензими
- косопад, прекомерно изпотяване (хиперхидроза), сърбеж, обрив
- мускулни крампи
- уголемяване на гърдите, бучки в гърдите, анормален клетъчен растеж в шийката на матката (цервикална дисплазия), генитално дисфункционално кървене, болка по време на полов акт, фиброкистозна мастопатия, обилна менструация, менструални нарушения, киста на яйчника, тазова болка, предменструален синдром, доброкачествен тумор на матката, контракции на матката, маточно / вагинално кървене, включително зацапване, вагинално течение, вулвовагинална сухота
- умора, раздразнителност, подуване на някои части на тялото, например глезените (оток)
- загуба на тегло, промени в кръвното налягане.
Редки нежелани реакции (между 1 и 10 потребители на 10 000)
- инфекция с кандида, орален херпес, възпалително заболяване на таза, съдово заболяване на окото, което прилича на гъбична инфекция (предполагаем синдром на очна хистоплазмоза), гъбична кожна инфекция (tinea versicolor), инфекция на пикочните пътища, бактериално възпаление на вагината
- задържане на вода, повишаване на определени кръвни мазнини (триглицериди)
- агресия, тревожност, чувство на нещастие, повишено сексуално желание, нервност, кошмари, безпокойство, нарушения на съня, стрес
- намалено внимание, усещане за "щифтове и игли", замаяност
- непоносимост към контактни лещи, сухи очи, подути очи
- инфаркт (миокарден инфаркт), сърцебиене
- кървене от разширени вени, ниско кръвно налягане, възпаление на повърхностни вени, болки във вените
- вредни кръвни съсиреци във вена или артерия, например: в крака или стъпалото (DVT), белия дроб (PE), инфаркт, инсулт, мини-инсулт или временни симптоми, подобни на инсулт, известни като преходна исхемична атака (TIA), кръвни съсиреци в черния дроб, стомаха / червата, бъбреците или окото.
Шансът за образуване на кръвен съсирек може да бъде по -висок, ако имате някакви други състояния, които увеличават този риск (вижте точка 2 за повече информация относно състояния, които увеличават риска от образуване на кръвни съсиреци и симптомите на кръвен съсирек).
- запек, сухота в устата, лошо храносмилане, киселини
- чернодробни възли (фокална нодуларна хиперплазия), хронично възпаление на жлъчния мехур
- алергични кожни реакции, жълто-кафяви петна (хлоазма) и други нарушения на пигментацията, хирзутизъм, прекомерен растеж на косата, кожни нарушения като: дерматит и невродермит, пърхот и мазна кожа (себорея) и други кожни състояния
- болки в гърба, челюст, усещане за тежест
- болка в пикочните пътища
- необичайно кървене при абстиненция, доброкачествени гърди, рак на гърдата в ранен стадий, киста на гърдата, отделяне на гърдата, полип на шийката на матката, зачервяване на шийката на матката, кървене по време на полов акт, спонтанно отделяне на кърма, генитален секрет, ниска менструация, забавяне на менструацията, разкъсване на киста на яйчника, неприятна миризма вагинално течение, усещане за парене във вулвата и влагалището, вулвовагинален дискомфорт
- увеличени лимфни жлези,
- астма, затруднено дишане, кървене от носа
- болка в гърдите, умора и общо неразположение, треска
- Необичайна цитонамазка (намазка) на шийката на матката
Допълнителна информация (взета от дневниците, водени от жените по време на клинично проучване с Qlaira) за възможните странични ефекти „нередовна менструация (с тежко нередовно кървене)“ и „без менструация“ може да бъде намерена в разделите „Междуменструално кървене“ и „Какво да правите направете, ако не настъпи менструация на 26 -ия ден или следващите дни ".
В допълнение към изброените по -горе странични ефекти, нодозумен еритем, мултиформен еритем, отделяне на гърдата и свръхчувствителност са се появили при потребители на комбинирани хапчета, съдържащи етинилестрадиол. Въпреки че тези симптоми не са докладвани по време на клинични изпитвания с Qlaira, не може да се изключи възможността те да се появят по време на лечението.
Докладване на странични ефекти
Ако получите някакви нежелани реакции, говорете с Вашия лекар или фармацевт.Това включва всички възможни нежелани реакции, които не са изброени в тази листовка. Можете също да съобщите нежелани реакции директно чрез националната система за съобщаване на адрес https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse.С докладването на странични ефекти можете да помогнете да предоставите повече информация за безопасността на това лекарство.
Срок на годност и задържане
Съхранявайте това лекарство на място, недостъпно за деца.
Този лекарствен продукт не изисква специални условия за съхранение.
Не използвайте това лекарство след срока на годност, отбелязан върху опаковката след "Годен до:". Срокът на годност се отнася до последния ден от месеца.
Лекарствата не трябва да се изхвърлят чрез отпадъчни води или битови отпадъци. Попитайте Вашия фармацевт как да изхвърлите лекарствата, които вече не използвате. Това ще помогне за опазването на околната среда.
Състав и лекарствена форма
Какво съдържа KLAIRA
Активните съставки са естрадиол валерат или естрадиол валерат, комбиниран с диеногест.
Една опаковка (28 филмирани таблетки) на Qlaira съдържа 26 активни таблетки с 4 различни цвята в 1-ви, 2-ри, 3-ти и 4-ти ред и 2 бели неактивни таблетки в 4-ти ред.
Състав от цветни таблетки, съдържащи една или две активни съставки:
- 2 тъмножълти таблетки, всяка съдържаща 3 mg естрадиол валерат,
- 5 червени таблетки, всяка от които съдържа 2 mg естрадиол валерат и 2 mg диеногест,
- 17 светложълти таблетки, всяка от които съдържа 2 mg естрадиол валерат и 3 mg диеногест,
- 2 тъмночервени таблетки, всяка съдържаща 1 mg естрадиол валерат.
Състав на неактивните бели таблетки:
Тези таблетки не съдържат никакви активни съставки.
Помощните вещества на цветните таблетки, съдържащи активните съставки, са:
Ядро на таблетката: лактоза монохидрат, царевично нишесте, прежелатинизирано царевично нишесте, повидон К25 (Е1201), магнезиев стеарат (Е572).
Покритие на таблетката: хипромелоза тип 2910 (E464), макрогол 6000, талк (E553b), титанов диоксид (E 171), червен железен оксид (E172) и / или жълт железен оксид (E172).
Другите съставки на белите неактивни таблетки са:
Ядро на таблетката: лактоза монохидрат, царевично нишесте, повидон К25 (Е1201), магнезиев стеарат (Е572).
Покритие на таблетката: хипромелоза тип 2910 (E464), талк (E553b), титанов диоксид (E171).
Как изглежда KLAIRA и какво съдържа опаковката
Таблетките Qlaira са филмирани таблетки; сърцевината на таблета е покрита с покритие.
Една опаковка (28 филмирани таблетки) на Qlaira съдържа 2 тъмножълти таблетки на 1-ви ред, 5 червени таблетки на 1-ви ред, 17 светложълти таблетки на 2-ри, 3-ти и 4-ти ред, 2 тъмночервени таблетки на 4-ти ред . 1 -ви ред и 2 неактивни бели таблетки в 4 -ти ред.
Тъмножълтата таблетка е кръгла, с двойно изпъкнали лица, върху една от които буквите "DD" са отпечатани в правилен шестоъгълник.
Червената таблетка е кръгла, с двойно изпъкнали лица, върху една от които буквите "DJ" са отпечатани в правилен шестоъгълник.
Светложълтата таблетка е кръгла, с двойно изпъкнали лица, върху една от които буквите "DH" са отпечатани в правилен шестоъгълник.
Тъмночервената таблетка е кръгла, с двойно изпъкнали лица, върху една от които буквите "DN" са отпечатани в правилен шестоъгълник.
Бялата (неактивна) таблетка е кръгла, с двойно изпъкнали лица, върху една от които буквите "DT" са отпечатани в правилен шестоъгълник.
Qlaira се предлага в опаковки от 1, 3 и 6 блистера, всяка с 28 таблетки. Не всички опаковки могат да бъдат пуснати на пазара.
Източник на листовката: AIFA (Италианска агенция по лекарствата). Съдържание, публикувано през януари 2016 г. Наличната информация може да не е актуална.
За да имате достъп до най-актуалната версия, препоръчително е да получите достъп до уебсайта на AIFA (Италианска агенция по лекарствата). Отказ от отговорност и полезна информация.
01.0 ИМЕ НА ЛЕКАРСТВЕНИЯ ПРОДУКТ
ТАБЛЕТКИ KLAIRA, ПОКРИТИ С ФИЛМ
02.0 КАЧЕСТВЕН И КОЛИЧЕСТВЕН СЪСТАВ
Всяка календарна опаковка (28 филмирани таблетки) съдържа в следния ред:
2 тъмножълти таблетки, всяка от които съдържа 3 mg естрадиол валерат,
5 червени таблетки, всяка от които съдържа 2 mg естрадиол валерат и 2 mg диеногест,
17 светложълти таблетки, всяка от които съдържа 2 mg естрадиол валерат и 3 mg диеногест,
2 тъмночервени таблетки, всяка от които съдържа 1 mg естрадиол валерат,
2 бели таблетки, които не съдържат активни съставки.
Помощно вещество с известен ефект: лактоза (не повече от 50 mg на таблетка).
За пълния списък на помощните вещества вижте точка 6.1.
03.0 ЛЕКАРСТВЕНА ФОРМА
Филмирана таблетка (таблетка).
Кръгла, тъмно жълта филмирана таблетка с двойно изпъкнали лица, едната от които е с релефни букви "DD" в правилен шестоъгълник.
Кръгла, червена, филмирана таблетка с двойно изпъкнали лица, едната от които е с релефни букви „DJ“ в правилен шестоъгълник.
Кръгла, светложълта, филмирана таблетка с двойно изпъкнали лица, едната от които е с релефни букви "DH" в правилен шестоъгълник.
Кръгла, тъмночервена, филмирана таблетка с двойно изпъкнали лица, едната от които е с релефни букви "DN" в правилен шестоъгълник.
Кръгла, бяла, филмирана таблетка с двойно изпъкнали лица, едната от които е с релефни букви "DT" в правилен шестоъгълник.
04.0 КЛИНИЧНА ИНФОРМАЦИЯ
04.1 Терапевтични показания
Орална контрацепция.
Лечение на тежки менструални потоци, при липса на органична патология, при жени, които желаят да прибягнат до орална контрацепция.
Решението за предписване на Qlaira трябва да отчита текущите рискови фактори на отделната жена, особено тези, свързани с венозна тромбоемболия (ВТЕ) и сравнението между риска от ВТЕ, свързан с Qlaira, и този, свързан с други комбинирани хормонални контрацептиви (КОК). (Вж. раздели 4.3 и 4.4).
04.2 Дозировка и начин на приложение
Начин на приложение
Перорална употреба
Дозировка
Как да приемате KLAIRA
Таблетките трябва да се приемат по едно и също време всеки ден с малко количество течност, ако е необходимо, и в реда, в който се предлагат в блистерната опаковка. Необходимо е да се приема по една таблетка на ден в продължение на 28 последователни дни. Следващата опаковка се започва в деня след последната таблетка от предишната опаковка.Кръвотечение при оттегляне обикновено възниква по време на приема на последните таблетки от календарна опаковка и може да не е приключило преди началото на новата календарна опаковка. При някои жени кървенето започва, след като приемат първите таблетки от новия календарен пакет.
Как да започнете лечение с KLAIRA
• Без предишна употреба на хормонални контрацептиви (през предходния месец).
Първата таблетка трябва да се приеме през първия ден от естествения цикъл (т.е. първия ден от менструацията).
• Преминаване от комбиниран хормонален контрацептив (комбиниран орален контрацептив), вагинален пръстен или трансдермален пластир.
Qlaira трябва да се започне в деня след последната активна таблетка (последната таблетка, съдържаща активните вещества) от предишния КОК. В случай на вагинален пръстен или трансдермален пластир, Qlaira трябва да започне в деня на отстраняване.
• Промяна от метод само с прогестаген (хапче само с прогестаген, инжекция, имплант) или от вътрематочна система, освобождаваща прогестоген (IUS).
Можете да преминете към Klaira по всяко време, ако използвате само прогестогенни хапчета (ако смените от имплант или IUS от деня на отстраняването му; от продукт за инжекционна употреба от момента на инжектиране по-късно), но във всички в тези случаи трябва да се използва допълнителен бариерен метод на контрацепция през първите 9 дни от приема на Qlaira.
• След аборт през първия триместър на бременността.
Можете да започнете веднага. В този случай не е необходим допълнителен контрацептивен метод.
• След раждане или след аборт през втория триместър на бременността.
За кърмещи жени вижте точка 4.6.
Препоръчително е да започнете между 21 -ия и 28 -ия ден след раждането или след аборт през втория триместър на бременността. В случай на по -късно начало, трябва да се използва допълнителен бариерен метод на контрацепция през първите 9 дни от приема на Qlaira. Ако обаче сте имали полов акт, бременността трябва да бъде изключена, преди да започнете да използвате комбинирания орален контрацептив, или трябва да изчакате първата си менструация.
Ако пропуснете таблетка
Всички пропуснати плацебо (бели) таблетки трябва да се изхвърлят, за да не се удължи интервалът между активните периоди на приемане на таблетки.
Следните съвети се отнасят само до забравяне на активни таблетки:
Ако сте закъснели с приема на таблетка с по -малко от 12 часа, контрацептивната защита не се намалява. Трябва да вземете таблетката веднага щом си спомните и след това да вземете следните таблетки в обичайното време.
Ако сте закъснели с приемането на таблетка повече от 12 часа, може да се намали контрацептивната защита. Трябва да вземете забравената таблетка веднага щом си спомните, дори ако това означава да приемате две таблетки заедно. След това трябва да продължите да приемате таблетките. обичайно време.
В зависимост от деня на цикъла, в който таблетката е забравена (вижте диаграмата по -долу за подробности), трябва да се използват допълнителни контрацептивни методи (например бариерен метод като презервативи) съгласно следните критерии:
Не трябва да се приемат повече от две таблетки в същия ден.
Ако една жена е забравила да започне нов календарен пакет или е забравила да вземе една или повече таблетки в рамките на 3-9 дни от календарната опаковка, тя може вече да е забременяла). Колкото повече таблетки са забравени (от тези с двете свързани активни вещества в дни 3-24) и колкото по-близо сте до дните на плацебо таблетките, толкова по-висок е рискът от бременност.
Ако жената е забравила таблетки и впоследствие не изпитва кървене при оттегляне в края на календарната опаковка или в началото на новата опаковка, трябва да се има предвид възможността за бременност.
Педиатрична популация
Няма налични данни за употреба при юноши под 18 години.
Предупреждения в случай на стомашно -чревни нарушения
В случай на тежки стомашно -чревни смущения (напр. Повръщане или диария), абсорбцията може да бъде нарушена и трябва да се използват допълнителни контрацептивни методи.
Ако повръщане настъпи в рамките на 3-4 часа след приемането на активна таблетка, следващата таблетка трябва да се вземе възможно най-скоро.Тази таблетка трябва да се вземе в рамките на 12 часа от обичайното време за приемане на таблетките. се прилагат инструкциите, дадени в точка 4.2 „Ако пропуснете таблет“.
Ако жената не желае да промени обичайния си график за прием на таблетки, тя ще трябва да вземе необходимата (ите) таблетка (и) от друга опаковка.
04.3 Противопоказания
Комбинираните хормонални контрацептиви (КОК) не трябва да се използват при следните състояния. Ако някое от тези състояния се появи за първи път по време на употребата на КОК, лечението трябва незабавно да се спре.
• Наличие или риск от венозна тромбоемболия (ВТЕ)
- Венозна тромбоемболия - текуща (с прием на антикоагуланти) или предишна ВТЕ (напр. Дълбока венозна тромбоза [ДВТ] или белодробна емболия [РЕ])
- Известна наследствена или придобита предразположеност към венозна тромбоемболия, като резистентност към активиран протеин С (включително фактор V Leiden), дефицит на антитромбин III, дефицит на протеин С, дефицит на протеин S
- Тежка операция с продължително обездвижване (вж. Точка 4.4)
- Висок риск от венозна тромбоемболия поради наличието на множество рискови фактори (вж. Точка 4.4)
• Наличие или риск от артериална тромбоемболия (ATE)
- артериална тромбоемболия - настояща или предишна артериална тромбоемболия (напр. Миокарден инфаркт) или продромални състояния (напр. Ангина пекторис)
- Цереброваскуларно заболяване - настоящ или предишен инсулт или продромални състояния (напр. Преходна исхемична атака (TIA))
- Известна наследствена или придобита предразположеност към артериална тромбоемболия, като хиперхомоцистеинемия и антифосфолипидни антитела (антикардиолипинови антитела, лупусов антикоагулант)
- История на мигрена с фокални неврологични симптоми
- Висок риск от артериална тромбоемболия поради наличието на множество рискови фактори (вж. Точка 4.4) или наличието на сериозен рисков фактор като:
• захарен диабет със съдови симптоми
• тежка хипертония
• тежка дислипопротеинемия
• панкреатит или неговата история, ако са свързани с тежка хипертриглицеридемия;
• съществуващи или предишни тежки чернодробни заболявания, докато стойностите на чернодробната функция се нормализират;
• настоящи или предишни тумори на черния дроб (доброкачествени или злокачествени);
• Известни или предполагаеми злокачествени заболявания, зависими от половите стероиди (напр. На половите органи или гърдата);
• вагинално кървене с неопределен характер;
• свръхчувствителност към активните вещества или към някое от помощните вещества, изброени в точка 6.1.
04.4 Специални предупреждения и подходящи предпазни мерки при употреба
Предупреждения
Ако са налице някое от условията или рисковите фактори, споменати по -долу, пригодността на Klaira трябва да се обсъди с жената.
В случай на влошаване или първа поява на някой от тези рискови фактори или състояния, жената трябва да се свърже с лекаря си, за да определи дали употребата на Qlaira трябва да се преустанови.
В случай на предполагаема или потвърдена ВТЕ или АТЕ, употребата на КОК трябва да се преустанови.
Няма епидемиологични проучвания за ефектите на комбинираните орални контрацептиви, съдържащи естрадиол / естрадиол валерат. Всички следните предупреждения и предпазни мерки са получени от клинични и епидемиологични данни за комбинирани орални контрацептиви, съдържащи етинилестрадиол. Не е известно дали тези предупреждения и предпазни мерки се отнасят за Qlaira.
• Нарушения на кръвообращението
Риск от венозна тромбоемболия (ВТЕ)
Използването на какъвто и да е комбиниран хормонален контрацептив (КОК) води до повишен риск от венозна тромбоемболия (ВТЕ) в сравнение с без употреба. Продуктите, съдържащи левоноргестрел, норгестимат или норетистерон, са свързани с по -нисък риск от ВТЕ. Все още не е известно как рискът, свързан с Qlaira, се сравнява с тези продукти с по -нисък риск. Решението да се използва продукт, различен от тези, свързани с по -нисък риск от ВТЕ, трябва да се вземе само след разговори с жената, за да се гарантира, че тя разбира риска от ВТЕ, свързан с КХК, как настоящите му рискови фактори влияят върху този риск и факта, че рискът от развитие на ВТЕ е най -висок през първата година от употребата. Има и някои доказателства, че рискът се увеличава, когато приемът на КОК се възобнови след пауза от 4 или повече седмици.
Около 2 от 10 000 жени, които не използват CHC и които не са бременни, ще развият ВТЕ за период от една година. При една жена обаче рискът може да бъде много по -висок, в зависимост от нейните основни рискови фактори (виж по -долу).
Епидемиологични проучвания при жени, използващи ниски дози комбинирани орални контрацептиви (
Смята се, че от 10 000 жени, които използват левоноргестрел-съдържащ CHC, около 6 ще развият ВТЕ за една година.
Все още не е известно дали рискът от ВТЕ, свързан с КОК, съдържащи диеногест в комбинация с естрадиол, е сравним с риска, свързан с КОК, съдържащи левоноргестрел.
Броят на ВТЕ годишно с ниски дози ХСК е по-нисък от очаквания брой при бременни или жени след раждане.
ВТЕ може да бъде фатално в 1-2% от случаите.
Много рядко се съобщава за тромбоза при потребители на CHC в други кръвоносни съдове, например чернодробни, мезентериални, бъбречни или ретинални вени и артерии.
Рискови фактори за ВТЕ
Рискът от венозни тромбоемболични усложнения при потребителите на КХК може да се увеличи значително, ако са налице допълнителни рискови фактори, особено ако има повече от един рисков фактор (вж. Таблицата).
Qlaira е противопоказан, ако една жена има няколко рискови фактора, които увеличават риска от венозна тромбоза (вж. Точка 4.3). Ако една жена има повече от един рисков фактор, възможно е повишеният риск да е по-голям от сумата на отделните фактори; в този случай трябва да се вземе предвид общият й риск от ВТЕ. Ако съотношението полза-риск се счита за отрицателно , не трябва да се предписва СНС (вж. точка 4.3).
Няма съгласие относно възможната роля на разширените вени и повърхностния тромбофлебит в началото и прогресията на венозна тромбоза.
Трябва да се има предвид повишеният риск от тромбоемболия по време на бременност, особено 6-седмичния период на пуерпериума (за информация относно "Бременност и кърмене" вижте точка 4.6.
Симптоми на ВТЕ (дълбока венозна тромбоза и белодробна емболия)
Ако се появят симптоми от този тип, жените трябва незабавно да потърсят медицинска помощ и да ги информират, че приемат ХСГ.
Симптомите на дълбока венозна тромбоза (ДВТ) могат да включват:
- едностранно подуване на крака и / или стъпалото или по протежение на вена в крака;
- болка или нежност в крака, които могат да се усетят само при изправяне или ходене;
- повишено усещане за топлина в засегнатия крак; кожа на крака, която е червена или обезцветена.
Симптомите на белодробна емболия (РЕ) могат да включват:
- внезапно и необяснимо начало на задух и учестено дишане;
- внезапна кашлица, която може да бъде свързана с хемоптиза;
- остра болка в гърдите;
- силно замайване или замаяност;
- ускорен или неравномерен сърдечен ритъм.
Някои от тези симптоми (като „задух“ и „кашлица“) са неспецифични и могат да бъдат тълкувани погрешно като по-чести или по-малко сериозни събития (например инфекции на дихателните пътища).
Други признаци на съдова оклузия могат да включват: внезапна болка, подуване или бледосиньо обезцветяване на един „крайник.
Ако оклузията се осъществи в окото, симптомите могат да варират от безболезнено замъгляване на зрението до загуба на зрение. Понякога загубата на зрение се случва почти веднага.
Риск от артериална тромбоемболия (ATE)
Епидемиологичните проучвания свързват употребата на ХСС с повишен риск от артериална тромбоемболия (инфаркт на миокарда) или от мозъчно -съдови инциденти (напр. Преходна исхемична атака, инсулт). Артериалните тромбоемболични събития могат да бъдат фатални.
Рискови фактори за ATE
Рискът от артериални тромбоемболични усложнения или мозъчно -съдов инцидент при потребителите на CHC се увеличава при наличието на рискови фактори (вж. Таблицата). Qlaira е противопоказан, ако една жена има един сериозен рисков фактор или множество рискови фактори за АТЕ, които увеличават риска от артериална тромбоза (вж. Точка 4.3). Ако една жена има повече от един рисков фактор, възможно е увеличаването на риска да е по-голямо от сумата на отделните фактори; в този случай трябва да се вземе предвид общият й риск. Ако се смята, че балансът полза-риск е отрицателен, не трябва да се предписва СНС (вж. точка 4.3).
Симптоми на ATE
Ако се появят симптоми от този тип, жените трябва незабавно да се свържат с медицински специалист и да ги информират, че приемат ХСК.
Симптомите на мозъчно -съдов инцидент могат да включват:
• внезапно изтръпване или слабост на лицето, ръката или крака, особено от едната страна на тялото;
• внезапно затруднено ходене, виене на свят, загуба на равновесие или координация;
• внезапно объркване, трудности при говорене или разбиране;
• внезапно затруднено виждане на едното или на двете очи;
• внезапна, тежка или продължителна мигрена без известна причина;
- загуба на съзнание или припадък със или без конвулсии.
Временните симптоми предполагат, че това е преходна исхемична атака (TIA).
Симптомите на миокарден инфаркт (МИ) могат да включват:
• болка, дискомфорт, натиск, тежест, усещане за притискане или пълнота в гърдите, ръката или под гръдната кост;
- дискомфорт, излъчващ към гърба, челюстта, гърлото, ръцете, стомаха;
• чувство на ситост, лошо храносмилане или задушаване;
• изпотяване, гадене, повръщане или замаяност;
• крайна слабост, безпокойство или задух;
• бърз или неравномерен сърдечен ритъм.
• Тумори
В някои епидемиологични проучвания се съобщава за повишен риск от рак на шийката на матката при употребяващи КОК за продължителни периоди (> 5 години), но все още е спорно до каква степен тези констатации се дължат на объркващите ефекти на сексуалното и друго поведение. Фактори като човешки папиломен вирус (HPV).
Мета-анализ на 54 епидемиологични проучвания съобщава за малко по-висок относителен риск (RR = 1,24) от диагнозата рак на гърдата при жени, използващи КОК. Този повишен риск постепенно изчезва след 10 години след спиране на употребата на КОК. Тъй като ракът на гърдата е рядкост при жени на възраст под 40 години, допълнителният брой диагностицирани случаи на рак на гърдата при жени, които използват или наскоро са използвали КОК, е малък по отношение на общия риск от рак на гърдата. Тези проучвания не дават доказателства за причинно -следствена връзка. Наблюдаваният повишен риск може да се дължи на по -ранна диагноза рак на гърдата при употребяващите КОК, биологичните ефекти на КОК или комбинация от двата фактора. Ракът на гърдата, диагностициран при употребяващите КОК, обикновено е по -малък. Клинично напреднал от формите, диагностицирани при жени, които никога не са ги използвали.
Доброкачествени чернодробни тумори и още по -рядко злокачествени чернодробни тумори са докладвани рядко при жени, приемащи КОК. В единични случаи, тези тумори са довели до животозастрашаващи интраабдоминални кръвоизливи. Ако жена, приемаща комбиниран орален контрацептив, изпитва силна болка в горната част на корема, уголемяване на черния дроб или признаци, предполагащи интраабдоминален кръвоизлив, наличието на рак на черния дроб трябва да се има предвид при диференциалната диагноза.
• Други условия
Жените с хипертриглицеридемия или с положителна фамилна анамнеза за състоянието могат да имат повишен риск от панкреатит, когато използват КОК.
Въпреки че са докладвани малки повишения на кръвното налягане при много жени, приемащи КОК, рядко се наблюдават клинично значими повишения. Въпреки това, ако по време на употребата на КОК се развие клинично значима хипертония и нивата на кръвното налягане останат повишени, е разумно лекарят да спре КОК и да лекува хипертонията. Ако се сметне за подходящо, употребата на КОК може да бъде възобновена, ако антихипертензивната терапия постигне нормални стойности на кръвното налягане.
Съобщава се за появата или влошаване на следните състояния както при бременността, така и при употребата на КОК, но доказателствата за връзка с употребата на КОК са неубедителни: жълтеница и / или сърбеж от холестаза; камъни в жлъчния мехур; порфирия; системен лупус еритематозус; хемолитично-уремичен синдром; Хорея на Sydenham, херпес гестация, загуба на слуха от отосклероза.
При жени с наследствен ангиоедем екзогенните естрогени могат да предизвикат или изострят симптомите на ангиоедем.
Остри или хронични нарушения на чернодробната функция може да изискват преустановяване на лечението с КОК, докато маркерите на чернодробната функция не се нормализират. Връщането на холестатичната жълтеница, вече настъпила по време на бременност или по време на предишно лечение със сексуални стероиди, изисква лечение. "Прекратяване на комбинираните орални контрацептиви.
Въпреки че КОК могат да имат ефект върху периферната инсулинова резистентност и глюкозния толеранс, няма данни за необходимостта от промяна на схемата на лечение при жени с диабет, използващи ниски дози КОК (съдържащи КОК).
По време на употребата на КОК се съобщава за влошаване на ендогенна депресия, епилепсия, болест на Crohn и улцерозен колит.
Понякога може да се появи хлоазма, особено при жени с анамнеза за хлоазма гравидарум. Жените със склонност към хлоазма трябва да избягват излагането на слънце или ултравиолетови лъчи по време на лечението с КОК.
Естрогенът може да причини задържане на вода и затова жените с бъбречна или сърдечна дисфункция трябва да бъдат наблюдавани внимателно. Жените с краен стадий на бъбречна недостатъчност трябва да бъдат внимателно наблюдавани, тъй като нивото на циркулиращите естрогени може да се увеличи след прилагане на Qlaira.
Този лекарствен продукт съдържа не повече от 50 mg лактоза на таблетка.Пациентите с редки наследствени проблеми на галактозна непоносимост, лактазен дефицит или глюкозо-галактозна малабсорбция, които са на диета без лактоза, трябва да вземат предвид това количество.
Медицински прегледи / посещения
Преди започване или възобновяване на употребата на Qlaira трябва да се вземе пълна анамнеза (включително фамилна анамнеза) и да се изключи бременността. Трябва да се измери кръвното налягане и да се извърши клиничен преглед, ръководен от противопоказания (вж. Точка 4.3) и предупреждения (вж. точка 4.4). Важно е да се привлече вниманието на жената към информация, свързана с венозна или артериална тромбоза, включително риска, свързан с Qlaira в сравнение с други КХК, симптоми на ВТЕ и АТЕ, известни рискови фактори и какво да се прави в случай съмнение за тромбоза.
Жената също трябва да бъде уведомена за необходимостта да прочете внимателно листовката и да следва съветите й. Честотата и видът на прегледите трябва да се основават на установените насоки и да бъдат адаптирани към индивидуалната жена.
Жените трябва да бъдат предупредени, че хормоналните контрацептиви не предпазват от ХИВ инфекции (СПИН) и други болести, предавани по полов път.
Намалена ефективност
Ефикасността на КОК може да бъде намалена в следните случаи: забравяне да се вземат активни таблетки (вж. Точка 4.2), стомашно-чревни смущения по време на приема на активни таблетки (вж. Точка 4.2) или съпътстващи лекарствени терапии (вж. Точка 4.5).).
Управление на цикъла
При всички КОК може да възникне нередовно кървене (зацапване или пробивно кървене), особено през първите месеци на употреба.Така оценката на всяко нередовно кървене става смислена след период на корекция от приблизително три курса на лечение.
Въз основа на дневници на пациенти от сравнително клинично проучване, процентът на жените на цикъл, които са имали междуменструално кървене, е 10-18% за потребителите на Qlaira.
Аменорея може да се появи дори при липса на бременност, докато се използва Qlaira.На базата на дневниците на пациентите, аменорея се среща в приблизително 15% от курсовете.
Ако Qlaira е бил приет съгласно указанията, дадени в точка 4.2, е малко вероятно жената да е бременна.две последователни курса, бременността трябва да бъде изключена преди да продължите да използвате Qlaira.
Ако нередовната загуба на кръв продължава или се появи след редовни цикли, трябва да се вземат предвид нехормонални причини и да се предприемат подходящи диагностични мерки за изключване на злокачествено заболяване или бременност. Такива мерки могат да включват изстъргване.
04.5 Взаимодействия с други лекарствени продукти и други форми на взаимодействие
Забележка: Трябва да се направи справка с обобщението на характеристиките на продукта на съпътстващото лекарство, за да се идентифицират потенциалните взаимодействия.
Проучвания за взаимодействия са провеждани само при възрастни.
Следните взаимодействия са докладвани в литературата за КОК като цяло или са изследвани в клинични проучвания с Qlaira.
• Ефекти на други лекарства върху Qlaira
Може да възникнат взаимодействия с лекарства, които индуцират микрозомни ензими, което води до повишен клирънс на половите хормони и което може да доведе до пробивно кървене и / или неуспешна контрацепция.
Управление
Ензимната индукция вече може да се наблюдава след няколко дни на лечение.Максималната ензимна индукция обикновено се наблюдава в рамките на няколко седмици. След прекратяване на терапията, ензимната индукция може да продължи приблизително 4 седмици.
Краткосрочно лечение
Жените, подложени на лечение с ензимни индуктори, трябва временно да използват бариерен метод или друг метод на контрацепция в допълнение към комбинирания орален контрацептив. Бариерният метод трябва да се използва през целия период на съпътстващ прием на лекарства и в продължение на 28 дни след прекратяване на терапията. Ако терапията продължи след края на активните таблетки от опаковката с КОК, плацебо таблетките трябва да се изхвърлят и да се започне следващата опаковка от КОК.
Продължително лечение
За жени, подложени на продължително лечение с индуктори на чернодробните ензими, се препоръчва друг надежден, нехормонален метод на контрацепция.
Вещества, които увеличават клирънса на КОК (намалена ефикасност на КОК от ензимни индуктори) напр.:
Барбитурати, карбамазепин, фенитоин, примидон, рифампицин, лекарството срещу HIV ритонавир, невирапин и ефавиренц и евентуално също фелбамат, гризеофулвин, оксикарбазепин, топирамат и продукти, съдържащи „жълт кантарион“ (Hypericum perforatum).
В клинично проучване рифампицин, мощен индуктор на цитохром Р450 (CYP) 3A4, е довел до значително намаляване на равновесните концентрации и системна експозиция на диеногест и естрадиол. Стационарната AUC (0-24 часа) на диеногест и естрадиол намалява съответно с 83% и 44%.
Вещества с променлив ефект върху клирънса на КОК:
Когато се прилагат едновременно с КОК, комбинации от инхибитори на HIV протеаза и ненуклеозидни инхибитори на обратната транскриптаза, включително комбинации с HCV инхибитори, могат да увеличат или намалят плазмените концентрации на естроген или прогестоген. Нетният ефект от тези промени в някои случаи може да бъде клинично значим.
Следователно трябва да се консултирате с информация за предписване на съпътстващи лекарства срещу HIV / HCV, за да се идентифицират потенциалните взаимодействия и всички свързани препоръки. Ако се съмнявате, жената, подложена на терапия с протеазни инхибитори или ненуклеозидни инхибитори на обратната транскриптаза, трябва да използва бариерен метод на контрацепция.
Вещества, които пречат на метаболизма на комбинирани хормонални контрацептиви (ензимни инхибитори):
Диеногест е субстрат на CYP3A4
Известни инхибитори на CYP3A4, като азолни противогъбични средства, циметидин, верапамил, макролиди, дилтиазем, антидепресанти и сок от грейпфрут, могат да повишат плазмените нива на диеногест.
В клинично проучване, оценяващо ефекта на инхибиторите на CYP3A4 (кетоконазол, еритромицин), стационарните плазмени нива на диеногест и естрадиол са повишени. Едновременното приложение със силния инхибитор на CYP3A4 кетоконазол води до 186% и 57% повишаване на AUC в равновесно състояние (0-24 часа) съответно на диеногест и естрадиол. Едновременното приложение на умерен инхибитор еритромицин повишава AUC (0-24 часа) в стационарно състояние на диеногест и естрадиол съответно с 62% и 33%. Клиничното значение на тези взаимодействия не е известно.
• Ефекти на Qlaira върху други лекарства
Оралните контрацептиви могат да повлияят на метаболизма на някои други активни съставки. Следователно плазмените и тъканните концентрации могат или да се увеличат (например циклоспорин), или да намалят (например ламотрижин).
Фармакокинетиката на нифедипин не се повлиява от едновременното приложение на 2 mg диеногест + 0,03 mg етинилестрадиол, като по този начин се потвърждават резултатите от in vitro проучвания, показващи, че е малко вероятно да настъпи инхибиране на CYP ензимите от Klaira. Терапевтична доза.
• Други форми на взаимодействие
Лабораторни изследвания
Употребата на контрацептивни стероиди може да повлияе на резултатите от някои лабораторни тестове, включително биохимични параметри, свързани с чернодробната, щитовидната, надбъбречната и бъбречната функция, плазмените нива на (транспортиращи) протеини, като свързващ глобулин. Кортикостероиди и липидни / липопротеинови фракции, параметри на въглехидратния метаболизъм и параметрите на коагулацията и фибринолизата Вариациите обикновено остават в рамките на лабораторните норми.
04.6 Бременност и кърмене
Бременност
Qlaira не трябва да се използва по време на бременност.
Ако по време на употребата на Qlaira настъпи бременност, по -нататъшният прием трябва да бъде спрян незабавно. Големите епидемиологични проучвания с комбинирани орални контрацептиви, съдържащи етинилестрадиол, не разкриват повишен риск от малформации при деца, родени от жени, които са използвали комбинирани орални контрацептиви преди бременност, нито тератогенни ефекти в случай на случайна употреба на комбинирани орални контрацептиви по време на бременност. . Проучванията при животни не показват риск от репродуктивна токсичност (вж. Точка 5.3).
Повишеният риск от тромбоемболия в следродилния период трябва да се вземе предвид при рестартиране на Qlaira (вж. Точки 4.2. И 4.4).
Време за хранене
Кърменето може да бъде повлияно от КОК, тъй като те могат да намалят количеството и да променят състава на кърмата.Поради това употребата на КОК не трябва да се препоръчва, докато отбиването не приключи. Малки количества от контрацептивните стероиди и / или техните метаболити могат да се екскретират в кърмата и да засегнат новороденото.
Плодовитост
Qlaira е показан за предотвратяване на бременност. За информация относно връщането към фертилитета вижте точка 5.1.
04.7 Ефекти върху способността за шофиране и работа с машини
Qlaira не влияе върху способността за шофиране или работа с машини.
04.8 Нежелани реакции
Таблицата по -долу изброява нежеланите реакции (АР), класифицирани по системен орган на MedDRA (MedDRA SOC). Списъкът съдържа термина MedDRA (версия 12.0), който е най -подходящ за описване на дадена нежелана реакция. Свързаните симптоми или състояния не са изброени, но все пак трябва да се имат предвид.
Честотите се основават на данни от клинични проучвания. Нежеланите реакции са регистрирани в 5 клинични изпитвания фаза III (n = 2266 жени с риск за бременност, n = 264 жени с дисфункционално маточно кървене, при липса на органична патология, които желаят да използват орална контрацепция) и се смята, че имат поне една възможна причинно -следствена връзка с използването на Klaira. Всички нежелани лекарствени реакции, изброени в категорията "редки", се срещат при 1-2 доброволци, с честота
N = 2530 жени (100.0%)
1, включително вулвовагинална кандидоза и цервикални гъбички, идентифицирани в проба
2 включително плач и емоционална лабилност
3 включително загуба на либидо
4 включително променено настроение и промени в настроението
5 включително главоболие при напрежение и синусово главоболие
6 включително мигрена с аура и мигрена без аура
7 включително подуване на корема, болка в горната част на корема, болка в долната част на корема
8 включително повишена аланин аминотрансфераза, повишена аспартат аминотрансфераза, повишена гамаглутамилтрансфераза
9 включително пустули от акне
10 включително генерализиран сърбеж и сърбящ обрив
11 включително макулен обрив
12 включително алергичен дерматит и уртикария
13 включително напрежението на кожата
14 включително болка в гърдите, чувствителност на гърдите, дискомфорт в зърната и болка
15 включително нередовна менструация
16 включително подуване на гърдите
17 включително вагинален кръвоизлив, генитален кръвоизлив и маточен кръвоизлив
18 включително периферен оток
19 включва повишаване на кръвното налягане и понижаване на кръвното налягане
Описание на някои нежелани реакции
Повишен риск от артериални и венозни тромботични и тромбоемболични събития, включително инфаркт на миокарда, инсулт, преходни исхемични атаки, венозна тромбоза и белодробна емболия, е наблюдаван при потребители на КХК и този риск е обсъден по -подробно в точка 4.4.
Появата на аменорея и вътременструално кървене въз основа на дневниците на пациентите е обобщена в точка 4.4 "Управление на цикъла'.
Следните сериозни нежелани събития, обсъдени в точка 4.4, са докладвани при жени, приемащи КОК „Специални предупреждения и предпазни мерки при употреба“:
• венозни тромбоемболични нарушения;
• артериални тромбоемболични нарушения;
• хипертония;
• чернодробни тумори;
• поява или влошаване на състояния, при които връзката с КОК е неубедителна: болест на Крон, улцерозен колит, епилепсия, мигрена, миома на матката, порфирия, системен лупус еритематозус, херпес гестация, хорея на Sydenham, хемолитичен синдром- уремия, холестатична жълтеница;
• хлоазма;
• Хронични или остри нарушения на чернодробната функция може да изискват преустановяване на приема на КОК, докато маркерите на чернодробната функция се върнат към нормалните граници;
• при жени с наследствен ангиоедем, екзогенните естрогени могат да предизвикат или изострят симптомите на ангиоедем.
Честотата на диагнозите рак на гърдата сред потребителите на КОК се е увеличила много леко. Тъй като ракът на гърдата е рядък при жени на възраст под 40 години, броят на допълнителните случаи е малък по отношение на общия риск от рак на гърдата. Не е известно дали има причинно -следствена връзка с употребата на КОК.За допълнителна информация вижте раздели 4.3 и 4.4.
В допълнение към нежеланите реакции, споменати по -горе, по време на лечението с комбинирани орални контрацептиви, съдържащи етинилестрадиол, са настъпили случаи на нодозумен еритем, мултиформен еритем, отделяне на гърдата и свръхчувствителност. Въпреки че тези симптоми не са докладвани по време на клиничните проучвания с Qlaira, не може да се изключи възможността те да се появят и по време на лечението с това лекарство.
Взаимодействия
Взаимодействието между орални контрацептиви и други лекарства (ензимни индуктори) може да причини пробивно кървене и / или неуспех на контрацепцията (вж. Точка 4.5).
Докладване на предполагаеми нежелани реакции
Съобщаването на предполагаеми нежелани реакции, настъпили след разрешаване на лекарствения продукт, е важно, тъй като позволява непрекъснато наблюдение на съотношението полза / риск на лекарствения продукт. От здравните специалисти се изисква да съобщават за всякакви предполагаеми нежелани реакции чрез националната система за докладване. "Адрес https: //www.aifa.gov.it/content/segnalazioni-reazioni-avverse.
04.9 Предозиране
Не са докладвани сериозни вредни ефекти от предозирането. Симптомите, които могат да възникнат при предозиране на активни таблетки, са: гадене, повръщане и при млади момичета лека загуба на кръв. Няма антидоти и лечението трябва да бъде симптоматично.
05.0 ФАРМАКОЛОГИЧНИ СВОЙСТВА
05.1 Фармакодинамични свойства
Фармакотерапевтична група: естроген-прогестоген последователни препарати.
ATC код: G03AB08.
В клиничните проучвания, проведени с Klaira в Европейския съюз и в САЩ / Канада, бяха изчислени следните индекси на Pearl:
Pearl Index (18-50 години)
Неизправност на метода: 0,42 (горна граница 95% CI 0,77)
Грешка на потребителя + грешка на метода: 0.79 (горна граница 95% CI 1.23)
Pearl Index (18-35 години)
Неизправност на метода: 0,51 (горна граница 95% CI 0,97)
Грешка на потребителя + грешка на метода: 1,01 (горна граница 95% CI 1,59)
Контрацептивният ефект на КОК се основава на взаимодействието на няколко фактора, като основните са инхибирането на овулацията, промените в цервикалната слуз и промените в ендометриума.
В проучване за инхибиране на овулацията с 3 цикъла, лечението с Qlaira води до потискане на развитието на фоликулите при повечето жени. По време на цикъла след лечение, активността на яйчниците се връща към нивата преди лечението.
Qlaira е формулиран с намаляваща доза естроген и увеличаване на дозата на прогестаген. Този режим може да се използва за лечение на тежки менструални течения при липса на органична патология, нарушение, понякога наричано дисфункционално маточно кървене (DUB).
За да се оцени безопасността и ефикасността на Qlaira при жени със симптоми на DUB, които желаят да използват орална контрацепция, са проведени две многоцентрови, рандомизирани, двойно-слепи, подобни проекти. Като цяло 269 жени са рандомизирани на лечение с Klaira и 152 с плацебо .
След 6 -месечно лечение се наблюдава намаляване на средната относителна загуба на менструална кръв (MBL) с 88%, от 142 ml на 17 ml, в групата Klaira, спрямо 24%, от 154 ml на 117 ml, в групата на плацебо .
След 6 -месечно лечение процентът на жените, които са напълно излекувани от симптомите на DUB, е 29% в групата на Klaira, срещу 2% в групата на плацебо.
Естрогенът, присъстващ в Klaira, е естрадиол валерат, естер на естествен човешки 17β-естрадиол (1 mg естрадиол валерат съответства на 0,76 mg 17β-естрадиол). Този естроген се различава от естрогените, които обикновено се използват в комбинираните орални контрацептиви, които са етинил естрадиол или неговия пролекарствен местранол, по липсата на етинилова група в позиция 17α.
Диеногест е производно на нортестостерон, лишен от андрогенна активност, но с антиандрогенна активност, равна на около една трета от тази на ципротеронов ацетат. Диеногест се свързва с прогестероновия рецептор на човешката матка само с 10% от „Относителния афинитет към прогестерона. ниският му афинитет към прогестероновия рецептор, диеногестът има мощен прогестогенен ефект in vivo.Диеногест няма значителна андрогенна, минералокортикоидна или глюкокортикоидна активност in vivo.
Хистологията на ендометриума е изследвана в подгрупа жени (n = 218) в клинично проучване след 20 курса на лечение. Не са открити аномалии.
05.2 Фармакокинетични свойства
• Диеногест
Абсорбция
След перорално приложение диеногест се абсорбира бързо и почти напълно. След перорално приложение на таблетка Qlaira, съдържаща 2 mg естрадиол валерат и 3 mg диеногест, се постигат максимални серумни нива от 90,5 ng / ml за приблизително 1 час. Бионаличността е приблизително 91%. Фармакокинетиката на диеногест е пропорционална на дозата в диапазона от 1-8 mg.
Едновременният прием на храна няма клинично значим ефект върху скоростта или степента на абсорбция.
Разпределение
Относително висока фракция, равна на 10%, присъства в плазмата в свободна форма, докато около 90% е неспецифично свързана с албумин. Диеногест не се свързва със специфични транспортни протеини SHBG и CBG. Обемът на разпределение в стационарно състояние (Vd, SS) на диеногест е 46 1 след интравенозно приложение на 85 мкг 3Н-диеногест.
Биотрансформация
Диеногест се метаболизира почти напълно чрез метаболитните пътища, вече известни за стероиди (хидроксилиране, конюгиране), главно чрез CYP3A4. Фармакологично неактивните метаболити се екскретират бързо, така че диеногестът е най-голямата фракция, присъстваща в плазмата, представляваща около 50% от циркулиращите съединения, получени от диеногест.
Общият клирънс след интравенозно приложение на 3Н-диеногест е равен на 5,1 l / h.
Елиминиране
Плазменият полуживот на диеногест е приблизително 11 часа. Диеногест се метаболизира екстензивно и само 1% от лекарството се екскретира непроменено. Съотношението на екскреция с урина / фекалия е приблизително 3: 1 след перорално приложение на 0,1 mg / kg. След перорално приложение 42% от дозата се елиминира през първите 24 часа и 63% в рамките на 6 дни чрез бъбречна екскреция. Като цяло 86% от дозата се екскретира в урината и изпражненията след 6 дни.
Стационарни условия
Фармакокинетиката на диеногест не се влияе от нивата на SHBG.Стационарното състояние се достига след 3 дни при постоянна доза от 3 mg диеногест в комбинация с 2 mg естрадиол валерат. Минималните, максималните и средните стационарни концентрации на серумни диеноги T са съответно 11,8 ng / mL, 82,9 ng / mL и 33,7 ng / mL. Средното съотношение на натрупване за AUC (0-24 часа) е 1,24.
• Естрадиол валерат
Абсорбция
След перорално приложение естрадиол валерат се абсорбира напълно.Разцепването до естрадиол и валерианова киселина се случва по време на абсорбция от чревната лигавица или по време на първия чернодробен пасаж. Това води до увеличаване на естрадиола и неговите метаболити естрон и естриол.Максималната серумна концентрация на естрадиол от 70,6 pg / ml се достига между 1,5 и 12 часа след еднократно поглъщане на таблетката, съдържаща 3 mg естрадиол, оценена на 1 ден.
Биотрансформация
Валериановата киселина се метаболизира много бързо.След перорално приложение около 3% от дозата е директно бионалична като естрадиол.Естрадиолът е обект на забележим ефект при първо преминаване и значителна част от приложената доза вече се метаболизира в стомашно -чревната лигавица. Заедно с пресистемния метаболизъм в черния дроб, приблизително 95% от перорално приложената доза се метаболизира, преди да достигне системното кръвообращение. Основните метаболити са естрон, естрон сулфат и естрон глюкуронид.
Разпределение
В серума 38% от естрадиола се свързва с SHBG, 60% с албумин и 2-3% циркулира в свободна форма. Естрадиолът има умерено дозозависима индукционна активност върху серумните концентрации на SHBG.На 21 ден от цикъла на лечение SHBG е приблизително 148% от изходното ниво и намалява до приблизително 141% от изходното ниво на 28 ден (края на плацебо фазата) След интравенозно приложение се определя привиден обем на разпределение от приблизително 1,2 L / kg.
Елиминиране
Плазменият полуживот на циркулиращия естрадиол е приблизително 90 минути. След перорално приложение ситуацията е напълно различна. Поради големия циркулиращ набор от естроген сулфати и глюкурониди и ентеропатичната циркулация, крайният полуживот на естрадиола представлява сложен параметър, който зависи от всички тези процеси и е в диапазона от около 13-20 часа.
Естрадиолът и неговите метаболити се екскретират главно в урината, а около 10% се екскретира с изпражненията.
Стационарни условия
Фармакокинетиката на естрадиола се влияе от нивата на SHBG.При младите жени измерените нива на естрадиол в плазмата са резултат от ендогенния естрадиол и този, генериран от Qlaira. По време на фазата на лечение с 2 mg естрадиол валерат и 3 mg диеногест, равновесната максимална и средна серумна концентрация на естрадиол е съответно 66,0 pg / ml и 51,6 pg / ml. По време на 28-дневния цикъл се поддържат стабилни най-ниски концентрации на естрадиол, вариращи между 28,7 pg / mL и 64,7 pg / mL.
Специални популации
Фармакокинетиката на Qlaira не е проучена при пациенти с бъбречна или чернодробна недостатъчност.
05.3 Предклинични данни за безопасност
Неклиничните данни не разкриват особен риск за хората въз основа на конвенционални проучвания за токсичност при многократни дози, генотоксичност, репродуктивна токсичност.
Проучване за канцерогенност с диеногест при мишки и по -ограничено проучване при плъхове не показват увеличение на туморите.
Все пак трябва да се има предвид, че поради хормоналното си действие половите стероиди могат да стимулират растежа на определени хормонозависими тъкани и тумори.
06.0 ФАРМАЦЕВТИЧНА ИНФОРМАЦИЯ
06.1 Помощни вещества
06.2 Несъвместимост
Не е от значение.
06.3 Срок на валидност
5 години.
06.4 Специални условия на съхранение
Този лекарствен продукт не изисква специални условия за съхранение.
06.5 Естество на непосредствената опаковка и съдържанието на опаковката
Прозрачен блистер от PVC / алуминий в картонена опаковка с календар.
Пакети от:
1x28 таблетки.
3x28 таблетки.
6х28 таблетки.
Всяка календарна опаковка (28 филмирани таблетки) съдържа в следния ред: 2 тъмножълти таблетки, 5 червени таблетки, 17 светложълти таблетки, 2 тъмночервени таблетки и 2 бели таблетки.
Не всички опаковки могат да бъдат пуснати на пазара.
06.6 Инструкции за употреба и боравене
Неизползваното лекарство и отпадъците, получени от това лекарство, трябва да се изхвърлят в съответствие с местните разпоредби.
07.0 Притежател на разрешението за търговия
Bayer S.p.A. - Viale Certosa, 130 - 20156 Милано (MI)
08.0 НОМЕР НА РАЗРЕШЕНИЕТО ЗА ПОТРЕБЕНИЕ
1x28 филмирани таблетки AIC n. 038900015
3x28 филмирани таблетки AIC n. 038900027
6x28 филмирани таблетки AIC n. 038900039
09.0 ДАТА НА ПЪРВО РАЗРЕШЕНИЕ ИЛИ ПОДНОВЯВАНЕ НА РАЗРЕШЕНИЕТО
15 май 2009/03 ноември 2013 г.
10.0 ДАТА НА ПРЕГЛЕД НА ТЕКСТА
05/2015