Активни съставки: Тамсулозин (Тамсулозин хидрохлорид)
Pradif 0,4 mg твърди капсули с модифицирано освобождаване
Защо се използва Pradif? За какво е?
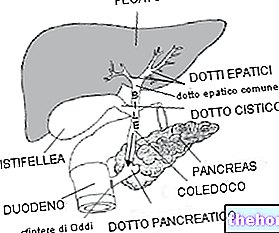
Активното вещество в Pradif е тамсулозин, селективен антагонист на α1A / α1D, който намалява мускулното напрежение в простатата и уретрата. Това позволява на урината да преминава по -бързо през уретрата, което улеснява уринирането. Намалява чувството за неотложност при уриниране.
Pradif се използва при мъже за лечение на симптоми на долните пикочни пътища, свързани с увеличена простата (доброкачествена хиперплазия на простатата). Тези нарушения могат да включват затруднено отделяне на урина (стесняване на струята), капене, спешност и увеличаване на честотата на уриниране. ден и нощ.
Противопоказания Когато Pradif не трябва да се използва
Не използвайте Pradif
- ако сте алергични (свръхчувствителни) към тамсулозин или към някоя от останалите съставки на Pradif. Свръхчувствителността може да се прояви като внезапно локално подуване на меките тъкани в тялото (например гърлото или езика), затруднено дишане и / или сърбеж и обрив (ангиоедем),
- ако имате тежки чернодробни проблеми,
- ако припаднете от спад на кръвното налягане при смяна на позиции (седнал или изправен).
Предпазни мерки при употреба Какво трябва да знаете, преди да приемете Pradif
Обърнете специално внимание при употребата на Pradif
- Необходими са периодични медицински прегледи, за да се проследи развитието на състоянието, за което се лекувате.
- Рядко може да възникне припадък при употребата на Pradif, както и при други лекарства от този тип.При първите признаци на замаяност или слабост трябва да седнете или да легнете, докато те изчезнат.
- Ако имате тежки бъбречни проблеми, моля уведомете Вашия лекар.
- Ако сте подложени или планирани за очна операция за помътняване на лещата (катаракта) или повишено налягане в окото (глаукома). Кажете на вашия офталмолог, ако преди сте приемали, приемате или планирате да приемате Pradif. Следователно специалистът може да вземе най -подходящите предпазни мерки по отношение на лекарството и хирургическата техника, която ще се използва. Попитайте Вашия лекар дали трябва да отложите или временно да спрете лечението с Pradif, преди да се подложите на очна операция за помътняване на лещата (катаракта) или повишено налягане в окото (глаукома).
Деца
Не давайте това лекарство на деца или юноши под 18 години, тъй като не е ефективно при тази популация.
Взаимодействия Кои лекарства или храни могат да променят ефекта на Pradif
Прием на Pradif с други лекарства
Приемът на Pradif с други лекарства, принадлежащи към същия клас (антагонисти на α1-адренорецепторите), може да причини нежелан спад на кръвното налягане. Pradif от тялото (напр. Кетоконазол, еритромицин).
Уведомете Вашия лекар или фармацевт, ако приемате или наскоро сте приемали други лекарства, включително и такива, отпускани без рецепта.
Прием на Pradif с храна и напитки
Pradif трябва да се приема след закуска или първото хранене за деня
Предупреждения Важно е да знаете, че:
Бременност, кърмене и фертилитет
Pradif не е показан за употреба при жени.
Съобщава се за анормална еякулация (нарушения на еякулацията) при мъжа. Това означава, че семенната течност не напуска тялото през уретрата, а навлиза в пикочния мехур (ретроградна еякулация) или че обемът на еякулацията е намален или отсъства (неуспех на еякулацията). Това събитие е безвредно.
Шофиране и работа с машини
Не е доказано, че Pradif влияе върху способността за шофиране или работа с машини или оборудване. Трябва обаче да имате предвид възможността да възникне замаяност, като в този случай не трябва да предприемате онези дейности, които изискват внимание.
Доза, метод и време на приложение Как да използвате Pradif: Дозировка
Винаги приемайте Pradif точно както Ви е казал Вашият лекар. Ако не сте сигурни, трябва да се консултирате с Вашия лекар или фармацевт. Обичайната доза е 1 капсула на ден, която трябва да се приема след закуска или след първото хранене за деня всеки ден.
Капсулата трябва да се поглъща цяла, без да се смачква или дъвче.
Pradif обикновено се предписва за дълги периоди от време. Ефектите върху пикочния мехур и уринирането се запазват след продължително лечение с Pradif.
Предозиране Какво да направите, ако сте приели твърде много Pradif
Ако сте приели повече от необходимата доза Pradif
Приемът на твърде много Pradif може да доведе до нежелан спад на кръвното налягане и повишаване на сърдечната честота, свързано с чувство на слабост.Ако сте приели твърде много дози Pradif, незабавно се консултирайте с Вашия лекар.
Ако сте пропуснали да приемете Pradif
Ако сте пропуснали да приемете доза Pradif, можете да я приемете по -късно през деня. Ако сте пропуснали ден, продължете да приемате дневната капсула в обичайното време.Никога не приемайте двойна доза, за да компенсирате пропуснатата.
Ако сте спрели приема на Прадиф
Когато лечението с Pradif бъде прекратено преждевременно, първоначалните симптоми могат да се появят отново. Ето защо, продължете да приемате Pradif толкова дълго, колкото Ви каже лекарят, дори ако симптомите Ви вече са изчезнали. Винаги се консултирайте с Вашия лекар, ако смятате, че тази терапия трябва да бъде преустановена.
Ако имате допълнителни въпроси относно употребата на това лекарство, попитайте Вашия лекар или фармацевт.
Странични ефекти Какви са страничните ефекти на Pradif
Както всички лекарства, Pradif може да има нежелани реакции, въпреки че не всеки ги получава.
Чести ефекти (по-малко от 1 на 10 случая, повече от 1 на 100 случая (1-10%)):
замаяност, особено при седене или изправяне.
Анормална еякулация (нарушение на еякулацията). Този симптом означава, че семенната течност не излиза от тялото през уретрата, а навлиза в пикочния мехур (ретроградна еякулация) или че обемът на семенната течност е намален или отсъства (неуспех на еякулацията.) Това събитие е безвреден.
Нечести ефекти (повече от 1 случай на 1000, по-малко от 1 случай на 100 (0,1-1%)):
главоболие, сърцебиене (сърцето бие по -често от нормалното и също се забелязва), понижаване на кръвното налягане, като например бързо ставане от седене или лежане, често свързано със замаяност, запушен или хрема (ринит), диария, гадене и повръщане, запек, слабост (астения), зачервяване на кожата (обрив), сърбеж и уртикария.
Редки ефекти (повече от 1 случай на 10 000, по-малко от 1 случай на 1000 (0,01-0,1%)):
припадък и случаи на внезапно локализирано подуване на меките тъкани на тялото (например на гърлото и езика), затруднено дишане със или без сърбеж и зачервяване на кожата (обрив), както често при алергична реакция (ангиоедем).
Много редки ефекти (по -малко от 1 случай на 10 000 (<0,01%)):
приапизъм (болезнена и продължителна неволна ерекция, изискваща незабавно медицинско лечение). Обрив, възпаление, образуване на мехури по кожата и / или лигавиците на устните, очите, устата, ноздрите или гениталиите (синдром на Stevens-Johnson).
Ефекти с неизвестна честота (честотата не може да бъде оценена от наличните данни):
- замъглено зрение
- зрително увреждане
- кървене от носа (епистаксис)
- тежки кожни обриви (еритема мултиформе, ексфолиативен дерматит)
- абнормен неправилен сърдечен ритъм (предсърдно мъждене, аритмия, тахикардия), затруднено дишане (диспнея).
- ако Ви предстои операция на очите поради помътняване на лещата (катаракта) или повишено налягане в окото (глаукома) и вече приемате или наскоро сте приемали Pradif, зеницата може да се разшири слабо и ириса (цветната кръгла част око) може да стане отпуснато по време на операцията.
- суха уста.
Ако някоя от нежеланите реакции стане сериозна или забележите други, неописани в тази листовка нежелани реакции, моля уведомете Вашия лекар или фармацевт.
Докладване на странични ефекти
Ако получите някакви нежелани реакции, говорете с Вашия лекар или фармацевт.Това включва всички възможни нежелани реакции, които не са изброени в тази листовка. Можете също да съобщите нежелани реакции директно чрез националната система за докладване на адрес www.agenziafarmaco.gov.it/it/responsabili.С докладването на странични ефекти можете да помогнете да предоставите повече информация за безопасността на това лекарство.
Срок на годност и задържане
Съхранявайте в оригиналната опаковка.
Съхранявайте Pradif на място, недостъпно за деца.
Не използвайте Pradif след срока на годност, отбелязан върху блистера и картонената опаковка след "Годен до:" (месец и година). Срокът на годност се отнася до последния ден от месеца.
Лекарствата не трябва да се изхвърлят чрез отпадъчни води или битови отпадъци. Попитайте Вашия фармацевт как да изхвърлите лекарствата, които вече не използвате. Това ще помогне за опазването на околната среда.
Състав и лекарствена форма
Какво съдържа Pradif
Активната съставка е тамсулозин хидрохлорид.
Другите съставки са: съдържание на капсули: микрокристална целулоза (Е460); метакрилова киселина-етил акрилатен съполимер (1: 1); полисорбат 80 (Е433); Натриев лаурил сулфат; триацетин (Е1518); калциев стеарат (E470a); талк (E553b). Черупка на капсулата: твърд желатин; индиго кармин (Е132); титанов диоксид (Е171); жълт железен оксид (Е172); червен железен оксид (Е172). Печатни мастила: шеллак (E904), пропиленгликол (E1520), черен железен оксид (E172).
Описание на това как изглежда Pradif и съдържанието на опаковката
Капсулите Pradif са оранжеви / маслинено зелени, обозначени с кодове и лого T0.4.
Капсулите Pradif са опаковани в полипропиленово-алуминиеви блистери, съдържащи се в картонена кутия.
Опаковката съдържа 10, 20, 30, 50, 60, 90, 100 или 200 капсули. Не всички видове опаковки могат да бъдат пуснати на пазара
Източник на листовката: AIFA (Италианска агенция по лекарствата). Съдържание, публикувано през януари 2016 г. Наличната информация може да не е актуална.
За да имате достъп до най-актуалната версия, препоръчително е да получите достъп до уебсайта на AIFA (Италианска агенция по лекарствата). Отказ от отговорност и полезна информация.
01.0 ИМЕ НА ЛЕКАРСТВЕНИЯ ПРОДУКТ
ПРАДИФ ТВЪРДИ КАПСУЛИ
02.0 КАЧЕСТВЕН И КОЛИЧЕСТВЕН СЪСТАВ
Всяка капсула с модифицирано освобождаване съдържа 0,4 mg тамсулозин хидрохлорид като активна съставка.
Помощни вещества: за пълния списък на помощните вещества вижте точка 6.1.
03.0 ЛЕКАРСТВЕНА ФОРМА
Оранжева / маслинено зелена капсула с модифицирано освобождаване, твърда, маркирана с код T0.4 и лого.
04.0 КЛИНИЧНА ИНФОРМАЦИЯ
04.1 Терапевтични показания
Симптоми на долните пикочни пътища (LUTS), свързани с доброкачествена простатна хиперплазия (ДПХ).
04.2 Дозировка и начин на приложение
Перорална употреба.
По една капсула на ден след закуска или след първото хранене за деня.
Капсулата трябва да се поглъща цяла и не трябва да се смачква или дъвче, тъй като това може да попречи на модифицираното освобождаване на активната съставка.
В случай на бъбречно увреждане не се налага коригиране на дозата.
В случай на лека до умерена чернодробна недостатъчност не се налага коригиране на дозата (вижте също точка 4.3 Противопоказания).
Педиатрична популация
Няма индикации за специфична употреба на Pradif при деца.
Безопасността и ефикасността на тамсулозин при деца
04.3 Противопоказания
Свръхчувствителност към тамсулозин хидрохлорид, включително медикаментозно индуциран ангиоедем или към някое от помощните вещества; анамнеза за ортостатична хипотония; тежка чернодробна недостатъчност.
04.4 Специални предупреждения и подходящи предпазни мерки при употреба
Както при другите антагонисти на а1-адренорецепторите, по време на лечението с Pradif може да настъпи намаляване на кръвното налягане в конкретни случаи, които рядко могат да доведат до синкоп. При първите признаци на ортостатична хипотония (замаяност, слабост) пациентът трябва да седне или да легне, докато симптомите изчезнат.
Преди започване на терапията с Pradif, пациентът трябва да бъде оценен за други състояния, които могат да причинят същите симптоми като доброкачествена хиперплазия на простатата. Преди започване на лечението и на редовни интервали след това трябва да се извърши ректално изследване и, ако е необходимо, определяне на простатно -специфичен антиген (PSA).
Лечението на пациенти с тежко бъбречно увреждане (креатининов клирънс под 10 ml / min) трябва да се обмисля с повишено внимание, тъй като лекарственият продукт не е проучен при тези пациенти.
Интраоперативен синдром на флопи ирис (IFIS, вариант на синдром на малка зеница) е наблюдаван по време на операция на катаракта и глаукома при някои пациенти на или преди лекувани с тамсулозин хидрохлорид.
IFIS може да увеличи риска от очни усложнения по време и след операцията.
Прекратяването на тамсулозин хидрохлорид 1-2 седмици преди операция на катаракта или глаукома се счита за емпирично полезно, но ползата от преустановяване на лечението все още не е установена.
IFIS е установен и при пациенти, които са спрели тамсулозин за по -дълъг период преди операцията.
Не се препоръчва започване на терапия с тамсулозин хидрохлорид при пациенти, за които се планира операция на катаракта или глаукома.
По време на предоперативната оценка, офталмологът и хирургичният екип трябва да преценят дали пациентът, който чака операция на катаракта или глаукома, се лекува или е бил лекуван с тамсулозин, за да се гарантира, че могат да бъдат предприети подходящи мерки за управление на IFIS по време на интервенцията.
Тамсулозин хидрохлорид не трябва да се прилага в комбинация със силни инхибитори на CYP3A4 при пациенти с лош метаболизиращ фенотип на CYP2D6.
Тамсулозин хидрохлорид трябва да се използва с повишено внимание в комбинация със силни и умерени инхибитори на CYP3A4 (вж. Точка 4.5).
04.5 Взаимодействия с други лекарствени продукти и други форми на взаимодействие
Проучвания за взаимодействия са провеждани само при възрастни.
Не са отбелязани взаимодействия, когато тамсулозин хидрохлорид се приема едновременно с атенолол, еналаприл или теофилин.
Едновременната употреба на циметидин причинява повишаване на плазмените нива на тамсулозин, докато фуроземид ги понижава; нивата на плазмената концентрация на тамсулозин обаче са в рамките на терапевтичния диапазон и поради това не е необходимо коригиране на дозата.
Инвитро диазепам, пропранолол, трихлорметиазид, хлормадинон, амитриптилин, диклофенак, глибенкламид, симвастатин и варфарин не променят свободната фракция на тамсулозин в човешката плазма. Тамсулозин не променя свободната фракция на диазепам, пропранолол, трихлорметиазид и хлормадинон.
Въпреки това, диклофенак и варфарин могат да увеличат скоростта на елиминиране на тамсулозин.
Едновременното приложение на тамсулозин хидрохлорид и силни инхибитори на CYP3A4 може да доведе до повишена експозиция на тамсулозин хидрохлорид. Едновременното приложение с кетоконазол (известен силен инхибитор на CYP3A4) води до повишаване на AUC и Cmax на тамсулозин хидрохлорид съответно с фактор 2.8 и 2.2.
Тамсулозин хидрохлорид не трябва да се прилага в комбинация със силни инхибитори на CYP3A4 при пациенти с лош метаболизиращ фенотип на CYP2D6.
Тамсулозин хидрохлорид трябва да се използва с повишено внимание в комбинация със силни и умерени инхибитори на CYP3A4.
Едновременното приложение на тамсулозин хидрохлорид и пароксетин, силен инхибитор на CYP2D6, води до повишаване на Cmax и AUC на тамсулозин съответно с 1,3 и 1,6 фактора, но тези увеличения не се считат за клинично значими.
Едновременната употреба на други а1-адренорецепторни антагонисти може да доведе до хипотензивни ефекти.
04.6 Бременност и кърмене
Pradif не е показан за употреба при жени.
Нарушения на еякулацията са наблюдавани при краткосрочни и дългосрочни клинични изпитвания с тамсулозин хидрохлорид. Случаи на нарушения на еякулацията, ретроградна еякулация и невъзможност за еякулация са докладвани в проучвания след разрешаване.
04.7 Ефекти върху способността за шофиране и работа с машини
Не са провеждани проучвания за способността за шофиране и работа с машини, но пациентът трябва да е наясно с възможността за замайване.
04.8 Нежелани реакции
* Наблюдава се в постмаркетинга
Вариант на синдрома на малките зеници, известен като „Синдром на интраоперативна флопи ирис“ (IFIS), свързан с терапията с тамсулозин, е наблюдаван по време на операция на катаракта и глаукома по време на постмаркетинговия период на наблюдение (вж. Също точка 4.4).
Постмаркетингов опит: В допълнение към нежеланите събития, изброени по-горе, се съобщава за предсърдно мъждене, аритмия, тахикардия и диспнея, свързани с употребата на тамсулозин.Тъй като тези спонтанно съобщени събития идват от постмаркетинговия опит по целия свят, тяхната честота и ролята на тамсулозин за причиняването им не могат да бъдат определени със сигурност.
Докладване на предполагаеми нежелани реакции
Съобщаването на предполагаеми нежелани реакции, настъпили след разрешаване на лекарствения продукт, е важно, тъй като позволява непрекъснато наблюдение на съотношението полза / риск на лекарствения продукт. От медицинските специалисти се изисква да съобщават за всякакви предполагаеми нежелани реакции чрез националната система за докладване. “Адрес www. agenziafarmaco.gov.it/it/responsabili.
04.9 Предозиране
Симптоми
Предозирането с тамсулозин хидрохлорид има потенциал да причини тежки хипотензивни ефекти.
Сериозни хипотензивни ефекти са наблюдавани при различни нива на предозиране.
Лечение
В случай на остра хипотония след предозиране, трябва да се предприемат бързи мерки за подпомагане на сърдечно -съдовата система.
Кръвното налягане и сърдечната честота могат да бъдат нормализирани, като пациентът лежи.
Ако това не е достатъчно, могат да се използват разширители на обема и, ако е необходимо, вазоконстриктивни лекарства. Трябва да се следи бъбречната функция и да се прилагат общи поддържащи мерки.
Диализата е малко полезна, тъй като тамсулозин се свързва силно с плазмените протеини. Някои мерки като повръщане могат да бъдат предприети, за да се предотврати абсорбцията.
В случай на поглъщане на големи дози, стомашната промивка може да бъде полезна и може да се приложи активен въглен и осмотично слабително средство, като натриев сулфат.
05.0 ФАРМАКОЛОГИЧНИ СВОЙСТВА
05.1 Фармакодинамични свойства
Фармакотерапевтична група: а1 антагонист на адренорецепторите.
ATC код: G04C A02.
Подготовка за изключително лечение на патологии на простатата.
Механизъм на действие:
тамсулозин селективно и конкурентно се свързва с постсинаптичните а1 адренорецептори, по -специално с подтиповете а1А и а1Д. Той кара гладките мускули на простатата и уретрата да се отпуснат.
Фармакодинамични ефекти:
pradif увеличава максималния поток на урината. Облекчава запушването, като отпуска гладките мускули на простатата и уретрата, като по този начин подобрява симптомите на изпразване.
Той също така подобрява симптомите на пълнене, при които нестабилността на пикочния мехур играе важна роля.
Тези ефекти върху симптомите на пълнене и изпразване се запазват по време на продължителна терапия. Необходимостта от операция или катетеризация се забавя значително.
Антагонистите на А1-адренорецепторите могат да намалят кръвното налягане чрез намаляване на периферното съпротивление. Не е наблюдавано клинично значимо понижение на кръвното налягане по време на клиничните изпитвания с Pradif.
Педиатрична популация
Двойно-сляпо, рандомизирано, плацебо-контролирано, дозово проучване е проведено при деца с невропатичен пикочен мехур. Общо 161 деца (на възраст 2-16 години) са рандомизирани и лекувани при 1 от 3 нива на доза тамсулозин (ниски [0,001 до 0,002 mg / kg], средни [0,002 до 0,004 mg / kg] и високи [0,004 до 0,008 mg / kg]), или с плацебо. Първичната крайна точка е броят на пациентите, при които налягането на детрузора в точката на изчезване (налягане на точката на изтичане на детрузора, LPP) намалява до стабилизиране на хидронефроза и хидроуретер и промяна в обема на урината, получена от катетеризацията и броя на изтичането на урина по време на катетеризацията, както е записано в дневниците за катетеризация. Няма значителна разлика между плацебо групата и която и да е от 3 -те групи тамсулозин нито за първичните, нито за вторичните крайни точки.Не е наблюдаван дозов отговор за всяко ниво на дозата.
05.2 Фармакокинетични свойства
Абсорбция
Тамсулозин хидрохлорид се абсорбира от червата и е почти напълно бионаличен.
Абсорбцията на тамсулозин хидрохлорид се намалява, като се приема близо до хранене.
Еднородна абсорбция може да се постигне, ако пациентът винаги приема Pradif след едно и също хранене.
Тамсулозин проявява линейна кинетика.
След еднократна доза Pradif в нахранено състояние, плазмените нива на тамсулозин достигат максимум за приблизително 6 часа и при стационарни условия, които се достигат след 5 дни лечение, Cmax е приблизително 2/3 по -висока от постигнатата след еднократна доза.
Това е отбелязано при пациенти в напреднала възраст и е разумно да се очаква същото при по -млади пациенти.
Съществуват значителни индивидуални различия в плазмените нива след еднократно и многократно дозиране.
Разпределение
При хората тамсулозин се свързва приблизително 99% с плазмените протеини.Обемът на разпределение е нисък (приблизително 0,2 l / kg).
Биотрансформация
Тамсулозин има слаб ефект на първо преминаване, тъй като се метаболизира бавно.
Тамсулозин присъства в плазмата главно под формата на непроменена активна съставка.
Метаболизира се в черния дроб.
На практика не се наблюдава индукция на микрозомалната чернодробна ензимна система, причинена от тамсулозин при плъхове.
Резултатите in vitro показват, че CYP3A4, а също и CYP2D6 участват в метаболизма, с евентуално незначителен принос към метаболизма на тамсулозин хидрохлорид от други CYP изоензими. Инхибирането на лекарствени метаболизиращи ензими CYP3A4 и CYP2D6 може да доведе до повишена експозиция на тамсулозин хидрохлорид (вж. Точки 4.4 и 4.5).
Нито един от метаболитите не е по -активен от оригиналния продукт.
Елиминиране
Тамсулозин и неговите метаболити се елиминират предимно в урината и приблизително 9% от дозата под формата на непроменено активно вещество.
След еднократна доза Pradif в условия на хранене и в стационарно състояние, елиминационният полуживот се оценява съответно на 10 и 13 часа.
05.3 Предклинични данни за безопасност
Проведени са проучвания за токсичност при единични и многократни дози при мишки, плъхове и кучета. Проучвания за репродукцията при плъхове, проучвания за канцерогенност при мишки и плъхове, също са разгледани проучвания за генотоксичност. in vivo и инвитро.
Общият токсикологичен профил, установен с по -високите дози тамсулозин, е в съответствие с известната фармакологична активност на лекарствата антагонисти на а1 -адренорецепторите.
При кучета при много високи дози електрокардиограмата се променя.Този отговор се счита за не клинично значим.
Тамсулозин не показва съответни генотоксични свойства.
"Съобщава се за повишена честота на пролиферативни промени във вимето на плъхове и женски мишки. Тези находки, които вероятно са медиирани от хиперпролактинемия и се проявяват само при високи дози, се считат за без значение".
06.0 ФАРМАЦЕВТИЧНА ИНФОРМАЦИЯ
06.1 Помощни вещества
Съдържание на капсулата:
микрокристална целулоза E460, метакрилова киселина - етил акрилатен съполимер (1: 1), полисорбат 80 E433, натриев лаурил сулфат, триацетин E1518, калциев стеарат E470a, талк E553b.
Капсула:
твърд желатин, индиго кармин Е132, титанов диоксид Е171, жълт железен оксид Е172, червен железен оксид Е172.
Мастило за печат:
шеллак E904, пропиленгликол E1520, черен железен оксид E172.
06.2 Несъвместимост
Не е от значение.
06.3 Срок на валидност
4 години.
06.4 Специални условия на съхранение
Съхранявайте в оригиналната опаковка.
06.5 Естество на непосредствената опаковка и съдържанието на опаковката
Полипропилен - алуминиеви блистери от 10 капсули, в картонени кутии с 10, 20, 30, 50, 60, 90, 100 и 200 капсули.
PVC / PVDC - алуминиев блистер с 5 капсули, в кутия с 50 капсули.
Не всички опаковки могат да бъдат пуснати на пазара.
06.6 Инструкции за употреба и боравене
Няма специални инструкции.
07.0 Притежател на разрешението за търговия
Boehringer Ingelheim International GmbH - Binger Strasse 173 - D 55216 Ingelheim am Rhein - Германия
Представител за Италия
Boehringer Ingelheim Italia S.p.A. - Via Lorenzini, 8 - 20139 Милано
08.0 НОМЕР НА РАЗРЕШЕНИЕТО ЗА ПОТРЕБЕНИЕ
Кутия с 20 капсули: A.I.C. N ° 030106013
Опаковка от 30 капсули: A.I.C. N ° 030106025
09.0 ДАТА НА ПЪРВО РАЗРЕШЕНИЕ ИЛИ ПОДНОВЯВАНЕ НА РАЗРЕШЕНИЕТО
27 септември 1996/12 юли 2006 г.
10.0 ДАТА НА ПРЕГЛЕД НА ТЕКСТА
10.06.2014.